“低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视。所以“低碳经济”正成为科学家研究的主要课题
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:(系数按顺序填在答题卷上)
___ C+ ___ KMnO4+ ____ H2SO4→____CO2↑+ ____MnSO4 + ____K2SO4+ ____H2O
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应
CO(g)+H2O(g)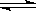 CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
| 实验组 |
温度℃ |
起始量/mol |
平衡量/mol |
达到平衡所需时间/min |
||
| CO |
H2O |
H2 |
CO |
|||
| 1 |
650 |
4 |
2 |
1.6 |
2.4 |
6 |
| 2 |
900 |
2 |
1 |
0.4 |
1.6 |
3 |
| 3 |
900 |
a |
b |
c |
d |
t |
①实验1中以v (CO2)表示的反应速率为 (取小数二位,下同)。
②该反应为 (填“吸”或“放”)热反应,实验2条件下平衡常数K= 。
(3)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH =-1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH =-566.0 kJ/mol
③ H2O(g) = H2O(l) ΔH =-44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
⑷某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置。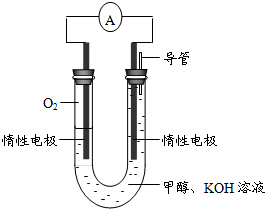
①该电池正极的电极反应为 。
②工作一段时间后,测得溶液的pH减小,该电池总反应的化学方程式为 。
(5)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10—9。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10—4mo1/L ,则生成沉淀所需CaCl2溶液的最小浓度为 。
在下列反应中:
| A.2F2+2H2O=4HF+O2 | B.2Na+2H2O=2NaOH+H2↑ |
| C.CaO+H2O=Ca(OH)2 | D.2H2O=2H2↑+O2↑ |
水只作氧化剂的是,水只作还原剂的是,水既作氧化剂又 作还原剂的是,水既不作氧化剂又不作还原剂的是。
作还原剂的是,水既不作氧化剂又不作还原剂的是。
除去括号中杂质,写出所加试剂的化学式与反应的离子方程式
(3)Fe2+(Cu2+),所加试剂________,离子方程式:________.
某溶液中可能有下列阴离子:SO42-、CO32-、Cl-。
(1)当溶液中存在大量H+时,溶液中不能大量存在的离子是________。
(2)当溶液中存在大量的Ba2+时,溶液中不能大量存在的离子是________。
(3)当溶液中存在大量________和________离子时,上述阴离子都不能大量存在.
483 g Na2SO4·10H2O中所含的Na+的物质的量是mol,SO42—的物质的量是mol,所含H2O分子的数目是个。
现有K 、O、S、H四种元素,选用其中一种或几种元素可组成符合下列要求的物质(酸、酸性氧化物、盐、X)。
(1)完成下列转化:(用化学方程式表示)
①酸 →盐: ;
;
②酸性氧化物 → 盐:;
(2)X在水溶液中电离成K+ 、H+、SO42-,则X的化学式为,X属于(填序号)
| A.酸 | B.碱 | C.盐 | D.氧化物 |
(3)设计两种实验方案(指出使用的试剂或方法) 鉴别Na2SO4和X:
鉴别Na2SO4和X:
方案1:。
方案2:。