常温时,下列溶液的pH或微粒的物质的量浓度关系不正确的是 ( )
A.将0.2 mol•L-1的某一元酸HA溶液和0.1 mol•L-1 NaOH溶液等体积混合后,混合液pH大于7,则反应后的混合液:2c(OH一)+c(A一)=2c(H+)+c(HA)
B.某溶液中存在的离子有Cl-、OH-、NH4+、H+,则离子浓度不一定是
c(Cl-)>c(NH4+)>c(H+)>c(OH-)
C.pH=3的二元弱酸H2R溶液与pH=11的NaOH溶液混合后,混合液的pH等于7,则反应后的混合液:2c(R2-)+c(HR一)=c(Na+)
D.某物质的溶液中由水电离出的c(H+)=1×10-a mol•L-1,若a>7时,则该溶液的pH一定为14-a
【原创】下列离子方程式正确的是
| A.钠和CuSO4溶液反应:2Na+Cu2+===Cu+2Na+ |
| B.用小苏打治疗胃酸过多:CO32-+ 2H+ = CO2↑ + H2O |
| C.澄清石灰水与少量小苏打溶液混合:Ca2+ +OH-+HCO3-= CaCO3↓+ H2O |
| D.往KAl(SO4)2溶液中滴入Ba(OH)2溶液至沉淀的物质的量最大: |
Al3++2SO42-+2Ba2++4OH-===AlO2-+2BaSO4↓+2H2O
【原创】下列分类的说法错误的是
| A.根据电解质在水溶液中能否完全电离将电解质分为强电解质和弱电解质 |
| B.根据分散系的稳定性大小,将分散系分为胶体、浊液和溶液 |
| C.依据有无电子转移,将化学反应分为氧化还原反应和非氧化还原反应 |
| D.根据化学反应的热效应,将化学反应分为放热反应、吸热反应 |
【原创】下列措施有利于节能减排、改善环境质量的有
| A.积极推行“限塑令”,用CO2合成聚碳酸酯等可降解塑料 |
| B.加速建设地铁、轻轨等轨道交通,促进城市一体化发展,减少汽车尾气排放 |
| C.改善能源结构,大力发展太阳能、风能等清洁能源 |
| D.焚烧废旧塑料,防止白色污染;使用填埋法处理生活垃圾 |
日用牙膏的主要成分有:活性物质、摩擦剂、甘油等。假设牙膏中摩擦剂成分为CaCO3、SiO2、Al(OH)3中的一种或几种物质组成,牙膏中其他成分均可溶于盐酸,且无气体产生。
(1)牙膏中添加甘油主要作用____。
为进一步探究牙膏中摩擦剂成分,进行了以下探究:
I.摩擦剂成分的定性检验:设计实验方案,验证假设。请写出实验步骤以及预期现象和结论(可不填满也可补充)。可选的试剂:稀盐酸,稀硫酸,NaOH溶液,澄清石灰水
| 实验步骤 |
预期现象和结论 |
| 步骤1:取适量牙膏样品,加水充分搅拌、过滤 |
有难溶物存在 |
| 步骤2: |
①有无色气泡产生,说明有CaCO3; ②_________,说明有______。 |
| 步骤3: |
|
| …… |
II.牙膏样品中碳酸钙的定量测定
利用如图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数。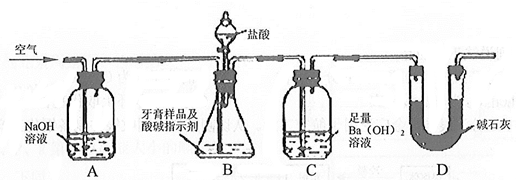
依据实验过程回答下列问题:
(2)实验过程中需持续缓缓通入空气。其主要作用 。
(3)仪器C中选择Ba(OH)2而不选择Ca(OH)2溶液原因:① 。② 。
(4)下列各项措施中,能提高测定准确度的是____(填标号)。
a.在加入盐酸之前,应排净装置内的CO2气体
b.缓慢滴加稀盐酸
c.在A-B之间增添盛有浓硫酸的洗气装置
d.在B-C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(5)实验中准确称取10. 00g样品三份,进行三次测定,洌得BaCO3平均质量为3.94g。则样品中碳酸钙的质量分数为_______。若改测定C中生成BaCO3质量为测定装置C在吸收CO2前后的质量差来确定CaCO3的质量分数,两方法测定的结果_______(填“相同”或“不同”),原因是 ___。
X、Y、Z、W均为短周期元素,它们在元素周期表中相对位置如图所示,若Z原子的最外层电子数是第一层电子数的3倍,下列说法正确的是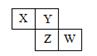
| A.Y单质与氢气反应较Z剧烈 |
| B.最高价氧化物对应水化物酸性W比Z强 |
| C.X单质氧化性强于Y单质 |
| D.X与W的原子核外电子数相差9 |