(共16分)在实验室里可用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。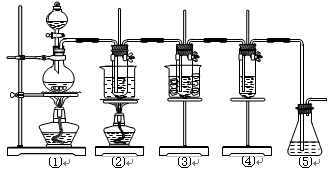
图中:①为氯气发生装置;②的试管里盛有15 mL 30% KOH溶液,并置于水浴中;③的试管里盛有15 mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。
请填写下列空白:
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过_____________(填写仪器名称)向烧瓶中加入适量的浓盐酸。实验时为了除去氯气中的氯化氢气体,可在①与②之间安装盛有_______(填写下列编号字母)的净化装置。
| A.碱石灰 | B.饱和食盐水 | C.浓硫酸 | D.饱和碳酸氢钠溶液 |
(2)比较制取氯酸钾和次氯酸钠的条件,二者的差异是:____________________________。
反应完毕经冷却后,②的试管中有大量晶体析出。下图中符合该晶体溶解度曲线的是_______(填写编号字母);从②的试管中分离出该晶体的方法是__________(填写实验操作名称)。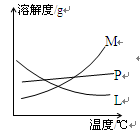
(3)本实验中制取次氯酸钠的离子方程式是______________________________________。
(4)实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白:
| 实验现象 |
原因 |
| 溶液最初从紫色逐渐变为_______色 |
氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 |
_______________________________ |
| 然后溶液从无色逐渐变为_______色 |
_______________________________ |
某研究性学习小组同学设计了如下图制取氯气(药品:MnO2和浓盐酸)并验证其性质的实验装置。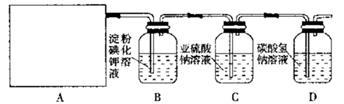
请回答下列问题:(1)该实验中A部分的装置是 (填写装置的序号)
(2)A中发生反应一段时间后,B中的现象是 ;
整套实验装置存在的明显缺陷是 。
(3)写出D装置中发生反应的离子方程式: 。
(4)请你帮该小组同学设计一个实验,证明洗气瓶C中的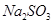 已被氧化(简述实验步骤): 。
已被氧化(简述实验步骤): 。
掌握仪器的名称、组装及使用方法是中学化学实验的基础,根据下图实验装置回答问题
(1)写出下列仪器的名称:① ,② ,④ 。
(2)仪器①~④中,使用时必须检查是否漏水的是 (填序号)。
(3)若利用装置Ⅰ分离酒精和水的混合物,还缺少的仪器 ,将仪器补充完整后进行的实验操作的名称为 ;②的进水口是 (填“f”或“g”)。
(4)现需配制250 mL、0.2 mol·L-1NaCl溶液,装置Ⅱ是某同学转移溶液的示意图,指出图中的错误之处:① ;② 。
草酸(H2C2O4)与高锰酸钾在酸性条件下能够发生如下反应:
2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,
【实验1】甲同学用8.00 mL 0.001 mol/L KMnO4溶液与5.00 mL 0.01 mol/L
H2C2O4溶液反应,研究不同条件对化学反应速率的影响。改变的条件如下:
| 组别 |
KMnO4溶液 /ml |
H2C2O4溶液 /ml |
10%硫酸体积/mL |
温度/℃ |
其他物质 |
| Ⅰ |
8.00 |
5.00 |
3.00 |
20 |
|
| Ⅱ |
8.00 |
5.00 |
3.00 |
30 |
|
| Ⅲ |
8.00 |
5.00 |
1.00 |
20 |
2.00 mL 蒸馏水 |
(1)如果研究温度对化学反应速率的影响,可用实验_________ 和________ 作对比(用Ⅰ~III表示)。
(2)对比实验Ⅰ和III,可以研究__________对化学反应速率的影响,实验Ⅲ中加入2.00 mL蒸馏水的目的是________________。
【实验2】乙同学在研究草酸与高锰酸钾在酸性条件下反应的影响因素时发现,草酸与酸性高锰酸钾溶液开始一段时间反应速率较慢,溶液褪色不明显,但不久后突然褪色,反应速率明显加快。
(1)针对上述现象,乙同学认为草酸与高锰酸钾反应放热,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你猜想还可能是 的影响。
(2)若用实验证明你的猜想,除了酸性高锰酸钾溶液和草酸溶液外,还需要选择的试剂最合理的是 (填字母)。A.硫酸钾 B.水 C.二氧化锰 D.硫酸锰
甲、乙两同学欲制取纯净的Fe(OH)2 ,根据右图所示的装置进行试验。A管中是Fe和稀硫酸, B管中是NaOH溶液,回答下列问题。
(1)同学甲:先夹紧止水夹a,使A管开始反应,一段时间后在B管中观察到的现象是:①液面上升,② 。此时B中发生现象②的化学反应方程式是: 。
(2)同学乙:先打开止水夹a,使A管中物质反应一段时间后,再夹紧止水夹a。同学乙在开始阶段进行的操作,主要的实验目的是: 。
(3)你认为 (填甲或乙)同学的实验可制取纯净的Fe(OH)2。
某化学小组为比较盐酸和醋酸的酸性,设计了如下实验方案。装置如图(夹持仪器略):
实验方案:在两试管中分别加入过量镁条,同时将两注射器中的溶液注入相应试管中,观察产生氢气的速率和体积。
(1)盐酸与镁反应的离子方程式为____________________。
(2)在上述实验方案中有一明显欠缺,该欠缺是____________。
(3)在欠缺已经得到改正的方案下,反应起始时,产生氢气的速率关系应是____________;最终产生氢气体积的关系应是_______________。
(4)实验中产生的氢气体积比理论值高,可能原因是_______________________。
(5)通过比较起始反应的速率可以得出的结论是______________。
(6)除上述方法外,还可以通过其他方向比较盐酸和醋酸的酸性,请写出其中的一种方法_________。