已知NO2和N2O4可以相互转化:2NO2(g)  N2O4(g) △H<0。现将一定量NO2和N2O4的混合气体通入体积为2 L的恒温密闭容器中,反应物浓度随时间变化关系如下图所示。
N2O4(g) △H<0。现将一定量NO2和N2O4的混合气体通入体积为2 L的恒温密闭容器中,反应物浓度随时间变化关系如下图所示。
(1)图中共有两条曲线X和Y,其中表示NO2浓度随时间变化的曲线是 ;a、b、c、d四个点中,表示化学反应处于平衡状态的点是 。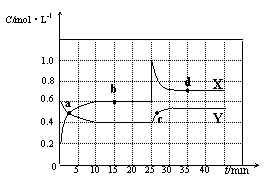
(2)①前10 min内用NO2表示的化学反应速率v(NO2)= mol·L-1·min-1。
②反应2NO2(g)  N2O4(g)在b点的平衡常数K(b)= 。
N2O4(g)在b点的平衡常数K(b)= 。
③反应2NO2(g)  N2O4(g)在d点的平衡常数K(d)与b点的平衡常数K(b)的关系:
N2O4(g)在d点的平衡常数K(d)与b点的平衡常数K(b)的关系:
K(d) K(b)(填“>”、“=”或“<”)。
(3)①据图分析,在25 min时采取的措施是 (填序号)。
| A.加入催化剂 | B.缩小容器体积 |
| C.加入一定量的NO2 | D.加入一定量的N2O4 |
②若在35 min时,保持温度不变,快速缩小容器的体积至1 L,气体的颜色变化过程是
(本题6分)Ⅰ.在某压强恒定的密闭容器中加入2 mol N2和4 mol H2,发生如下反应: N2(g)+3H2(g) 2NH3(g);ΔH=-92.4 kJ·mol-1。达到平衡时,体积为反应前的三分之二。求:
2NH3(g);ΔH=-92.4 kJ·mol-1。达到平衡时,体积为反应前的三分之二。求:
(1)达到平衡时,N2的转化率为____________。
(2)若向该容器中加入a mol N2、b mol H2、c mol NH3,且a、b、c均大于0,在相同条件下达到平衡时,混合物中各组分的物质的量与上述平衡相同。试比较反应放出的能量:(1)__________(2)(填“>”“<”或“=”)。
Ⅱ.若将2 mol N2和4 mol H2放入起始体积相同的恒容容器中,在与Ⅰ相同的温度下达到平衡。试比较平衡时NH3的浓度:Ⅰ____________Ⅱ(填“>”“<”或“=”)。
(本题10分)电化学在工业生产中有广泛应用。
(1)下图所示装置中,两玻璃管及烧杯中是滴有酚酞的NaCl饱和溶液C(Ⅰ)、C(Ⅱ)为多孔石墨电极。
①电解NaCl饱和溶液的化学方程式为:_________________________。
②接通S1后,C(Ⅰ)附近溶液变红,两玻璃管中均有气体生成。则电极C(Ⅰ)是_________(填“阳”或“阴”);C(Ⅱ)电极反应所得气体产物为_________。
③通电一段时间后(玻璃管中液面未脱离电极),断开S1,接通S2,电流表的指针发生偏转,此时电极C(Ⅰ)为_________(填“正”或“负”)极;C(Ⅰ)的电极反应为:______________________________________。
(2)若用此装置精炼粗铜,断开S2,接通S1,电解液选用CuSO4溶液;粗铜接电池的_________(填“正”或“负”)极,阴极发生的电极反应为:_____________________________。
(本题8分)汽车尾气是造成雾霾天气的重要原因之一。已知:
①N2(g)+O2(g) 2NO(g) ΔH1②2NO(g)+O2(g)
2NO(g) ΔH1②2NO(g)+O2(g) 2NO2(g)ΔH2
2NO2(g)ΔH2
③CO2(g) CO(g)+1/2O2(g)ΔH3④2CO(g)+2NO(g)
CO(g)+1/2O2(g)ΔH3④2CO(g)+2NO(g) N2(g)+2CO2(g)ΔH4
N2(g)+2CO2(g)ΔH4
请完成以下问题:
(1)请根据反应①②③,确定反应④中ΔH4=。
(2)根据图1,反应④的热化学方程式为:。
该反应在(填“高温”“低温”或“任意温度”)下有利于该反应正向自发。
(3)图2表示反应④的反应物NO、CO的起始物质的量比、温度对平衡时CO2的体积分数的影响。
①W、Y、Z三点的平衡常数的大小关系为:, X、Y、Z三点,CO的转化率由大到小的顺序是。
②T1℃时,在1L密闭容器中,0.1molCO和0.1molNO,达到Y点时,测得NO的浓度为0.02mol/L,则此温度下平衡常数K=(算出数值)。若此温度下,某时刻测得CO、NO、N2、CO2的浓度分别为0.01 mol/L、a mol/L、0.01 mol/L、0.04 mol/L,要使反应向正方向进行,a的取值范围为。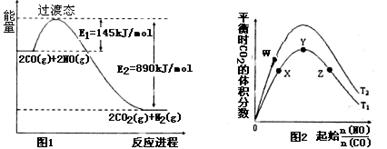
(4)恒温恒容时,反应④中NO、CO按一定比例投料,反应过程中CO浓度随时间的变化关系如图3所示,请在同一图中绘出N2浓度随时间的变化曲线。
研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)NO2可用水吸收,相应的化学反应方程式为。利用反应6NO2+ 8NH3 7N2+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是L。
7N2+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是L。
(2)已知:2SO2(g)+O2(g) 2SO3(g) ΔH=−196.6 kJ·mol-1
2SO3(g) ΔH=−196.6 kJ·mol-1
2NO(g)+O2(g) 2NO2(g)ΔH =−113.0 kJ·mol-1
2NO2(g)ΔH =−113.0 kJ·mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g)的ΔH =kJ·mol-1。
SO3(g)+NO(g)的ΔH =kJ·mol-1。
一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是。
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1 mol SO3的同时生成1 molNO2
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g) CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如下图所示。该反应ΔH0(填“>”或“ <”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是。
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如下图所示。该反应ΔH0(填“>”或“ <”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是。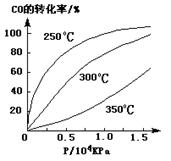
(本题8分)对于反应xA(g)+yB(g)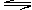 pC(g)+qD(g)压强与温度对C的质量分数的影响如图:
pC(g)+qD(g)压强与温度对C的质量分数的影响如图: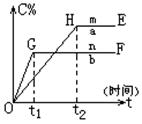
(1)若m、n表示不同温度,则mn,正反应为反应(填“放热”、“吸热”);
(2)若m、n表示不同压强,则mn,(x+y)(p+q)(填<、>、=);
(3)b曲线的OG段比a曲线的OH段陡的原是:;
(4)a曲线的HE段高于b曲线的GF段的原是:。