W、X、Y、Z均为短周期元素,W的最外层电子数与核外电子总数之比为7:17;X与W同主族;Y的原子序数是W和X的原子序数之和的一半;含Z元素的物质焰色反应为黄色。下列判断正确的是
A.金属性:Y>Z B氢化物的沸点:X>W
C.离子的还原性:X>W D原子及离子半径:Z>Y>X
下列化合物中沸点最低的是()
| A.己烷 | B.戊烷 | C.异戊烷 | D.新戊烷 |
三聚氰胺(结构式如图所示)是一种重要的化工原料,可用于阻燃剂、水泥减水剂和高分子合成等领域。一些不法分子却往牛奶中加入三聚氰胺,以提高奶制品的含氮量。下列说法正确的是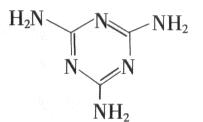

A.三聚氰胺是一种蛋白质 |
B.三聚氰胺是高分子化合物 |
C.三聚氰胺分子中含有碳碳双键 |
D.三聚氰胺的分子式为C3H6N6 |
等物质的量的下列烃,分别完全燃烧时,消耗O2最少的是( )
| A.C6H6 | B.CH4 | C.C2H4 | D.C7H8 |
下列化合物的分子式可能代表一种以上物质的是:()
| A.C3H8 | B.C4H10 | C.CH3Cl | D.CH2Br2 |
下列各组物质中,两者互为同分异构体的是 ( )
①CuSO4·3H2O和CuSO4·5H2O ②NH4CNO和CO(NH2)2
③C2H5NO2和NH2CH2COOH
④[Pu(H2O)4]Cl3和[Pu(H2O)2Cl2]·2H2O·Cl
| A.①②③ | B.②③④ | C.②③ | D.③④ |