在化学课上,甲同学将燃烧的钠迅速伸入到盛有CO2的集气瓶中,钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上附粘附着白色物质。
【提出问题】黑色颗粒和白色物质是什么?
【进行猜想】甲认为黑色颗粒是 ,白色物质可能是Na2O或 ;
乙同学还认为白色物质是氢氧化钠。
甲同学立刻认为乙同学的猜想是错误的,其理由是 。
【查阅资料】氧化钠为白色粉末,溶于水生成氢氧化钠:Na2O + H2O = 2NaOH
【实验探究】甲同学对白色物质进行实验探究。
| 实验方案 |
实 验 操 作 |
实验现象 |
结 论 |
| 方案1 |
取样品少量于试管中,加入适量水,振荡,样品 全部溶于水,向其中加入无色酚酞试液 |
溶液变成红色 |
白色物质 为Na2O |
| 方案2 |
①取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的CaCl2溶液 |
出现白色沉淀 |
白色物质 是 |
| ②静置片刻,取上层清液于试管中,滴加无色酚酞试液 |
无明显现象 |
【反思评价】丙同学认为方案1得到的结论不正确,理由是 。
【得出结论】钠在二氧化碳中燃烧的化学方程式为 。
通过以上探究,你还能获得哪些结论,请写出两条。(答对本小题将奖励4分,但全卷总分不超过60分)
② ,
② 。
实验装置及实验操作是化学实验的基本内容
(1)请将体现下列实验操作目的正确选项,填在对应的横线上
A. 防止药品污染 B. 防止试管破裂 C. 防止实验误差
加热试管时,先均匀加热后集中加热,滴管使用后,及时清洗并放在试管架上,量取液体时,视线与凹液面最低处保持水平。
(2)下列实验装置中均有水,请根据实验解释水在其中的主要作用
| 实验 装置 |
 硫在氧气中燃烧 |
 测定空气中氧气含量 |
 铁丝在氧气中燃烧 |
 水通电分解 |
| 主要作用 |
集气瓶中的水: 吸收反应放出的 热量及生成的气体 |
不少同学都被蚊虫叮咬过,感觉又痛又痒。同学们从化学课上知道:蚊虫叮咬时能在人的皮肤内分泌出蚁酸刺激皮肤。课外兴趣小组同学决定对蚁酸进行探究。
【提出问题】蚁酸的成分是什么?它有什么性质?
【查阅资料】蚁酸是一种有机酸,化学名称叫做甲酸,化学式为HCOOH;蚁酸在一定条件下会分解生成两种氧化物。
【实验探究一】探究蚁酸的酸性。
(1)向盛有蚁酸溶液的试管中滴加紫色石蕊试液,观察到溶液颜色变成____色,说明蚁酸溶液显酸性;
(2)将锌粒放入盛有蚁酸溶液的试管中,有气泡产生,该气体是____。
【实验探究二】探究蚁酸分解的两种产物。
(1)小芳同学根据蚁酸中含有________________元素,推测出生成物中含有水;
(2)另一种生成物是气体,小敏提出两种猜想:
猜想①:该气体是CO2猜想②:该气体是________________
他们将蚁酸分解产生的气体通过如下装置(铁架台已略去),观察现象。
I.实验时装置A中无明显变化,则猜想①_______
(填“成立”或“不成立”);
II.若猜想②成立,则装置B中的现象是_____________,
装置C中发生反应的化学方程式为 __________________。
【讨论交流】从环保角度看,该装置的缺陷是________
__________________,处理的方法是 _____________。
【拓展延伸】(1)当你被蚊虫叮咬后,在叮咬处涂抹一些物质可减轻痛痒。下列物质中,你不会选择的物质是_____________。
| A.氨水 | B.食醋 | C.肥皂水 | D.苏打水 |
(2)向某溶液中加入蚁酸有气泡产生,该气体能使澄清石灰水变浑浊,则该溶液中溶质的化学式可能是______________________________(只写一种)。
过氧化钠是化学中常见的一种药品,它是浅黄白色颗粒粉末。在空气中吸收水分和二氧化碳。易溶于水,与水中能发生反应生成氢氧化钠和过氧化氢,方程式:Na2O2+2H2O=2NaOH+H2O2,过氧化氢又能分解放出氧气。
(1)区分水和过氧化氢的实验方法是:__________,发生的反应方程式是:______________。
(2)某同学为了证明过氧化钠加入水中生成了氢氧化钠,在生成的溶液中滴加了几滴无色酚酞试液,观察到的现象是溶液先变红后褪为无色,请你对此现象进行探究。
【提出问题】:什么导致溶液先变红再褪色?
【猜想与假设】:
猜想1:甲同学“可能是无色酚酞溶液变质导致溶液褪色”;
猜想2:乙同学“可能是生成的过氧化氢使溶液褪色”。
【实验与结论】:
a:甲同学提出的猜想,立即遭到其他同学的反对,因为;
b:为了验证自己的猜想,乙同学设计了以下方案并实验验证:
| 实验步骤 |
实验现象 |
实验结论 |
| 取少量稀氢氧化钠溶液于试管中,滴加1—2滴酚酞试液,变红后 观察现象 |
溶液依然为红色 |
【讨论交流】:你还能提出不同的猜想吗?如果还能提出新的合理的假设和方案你将获得奖励分4分。(化学试卷总分不超过60分)
猜想3:。
方案3:
| 实验步骤 |
实验现象 |
实验结论 |
某同学对蜡烛(主要成分是石蜡)及其燃烧进行了探究。其实验步骤有:
①点燃蜡烛,紧贴烛芯将火柴梗放入火焰中约1秒后取出
②在火焰上方罩一个冷而干燥的小烧杯;
③用火柴去点白烟;
④切下一块石蜡,放入水中;
⑤熄灭蜡烛;
⑥迅速倒转烧杯,加入澄清石灰水,振荡。
请回答以下问题:
(1)参看下表的实验记录,以上操作步骤的正确排序是____________。
(2)按要求填写下列实验现象及其结论
| 探究步骤 |
对实验的观察和描述 |
| 点燃前 |
石蜡放入水中观察到的现象__________________________ |
| 燃着时 |
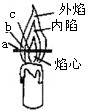 ①点燃蜡烛,把一根火柴梗放在蜡烛的火焰中,如图所示,约1s后取出可以看到火柴梗的_____(选填图中字母)处最先炭化。 ②干冷的烧杯内壁出现__________现象,澄清的石灰水__________。 |
| 熄灭后 |
吹灭蜡烛,观察到一缕白烟。 |
结论:蜡烛燃烧生成______________。
某化学兴趣小组的同学用洁净的塑料瓶从河中取回一定量的水样,然后进行如下研究分析: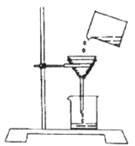
(1)将浑浊的河水样品倒入烧杯中,加入明矾粉末(吸附杂质,使杂质沉降)搅拌,静置一会儿;
(2)将静置后的河水采用如图所示的装置进行过滤,请问:图中还缺少的一种仪器是_____________,其作用是____________________________。
图中实验装置还存在的两处错误是:
_____________________________,____________________________。
(3)某同学用如图的装置进行过滤操作,实验后发现滤液仍浑浊,请你写出可能的两点原因:
①_____________________________________________;
②_____________________________________________。