X、Y、Z三种气体都能对大气造成污染,在工业上都可以用碱液吸收。已知X是化石燃料燃烧产物之一,是形成酸雨的主要物质;Y是一种单质,它的水溶液具有漂白作用;Z是硝酸工业和汽车尾气中的有害物质之一,能与水反应。请写出下列物质反应的化学方程式。
⑴ X在一定条件下与氧气反应__ ______
⑵ Y与氢氧化钠溶液的反应_____ ________
⑶ Z与水的反应___ _______________
氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,回答下列问题:
(1)氮的原子结构示意图为;
(2)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为;
(3)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)= N2O4 (1)△H1= -195kJ·mol-1
②N2H4 (1) + O2(g)= N2(g) + 2 H2O(g)△H2= -534.2kJ·mol-1
写出肼和N2O4反应的热化学方程式;
(4)肼一空气燃料电池是一种碱性电池,该电池放电时,负极生成无污染的气体,负极的反应式为。
下图甲池和乙池中的四个电极都是惰性材料,乙池溶液分层,下层为四氯化碳,上层溶液为盐溶液,呈中性,请根据图示回答下列问题: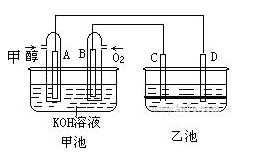
(1)通入甲醇的惰性电极的电极反应式为。若甲池可以充电,充电时A接电源的负极,此时B极发生的电极反应式为。
(2)在乙池反应过程中,可以观察到电极周围的溶液呈现棕褐色,反应完毕后,用玻璃棒搅拌溶液,则下层溶液呈现紫红色,上层接近无色, C极发生的电极反应式为。
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入20.00mL待测溶液到锥形瓶中。
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000 mol·L—1标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数。
③向锥形瓶中滴入酚酞作指示剂,进行滴定。滴定至指示剂刚好变色,且半分钟内颜色不再改变为止,测得所耗盐酸的体积为V1mL。
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL。
试回答下列问题:
(6)根据下列数据:
| 滴定次数 |
待测液体积(mL) |
标准盐酸体积(mL) |
|
| 滴定前读数(mL) |
滴定后读数(mL) |
||
| 第一次 |
20.00 |
0.50 |
25.40 |
| 第二次 |
20.00 |
4.00 |
29.10 |
请计算待测NaOH溶液的浓度为mol·L—1。
北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)。
(1)丙烷脱氢可得丙烯。
已知:C3H8(g)  CH4(g)+HC≡CH(g)+H2(g)△H1=+156.6kJ·mol-1
CH4(g)+HC≡CH(g)+H2(g)△H1=+156.6kJ·mol-1
CH3CH=CH2(g) CH4(g)+HC≡CH(g)△H2=+32.4kJ·mol-1
CH4(g)+HC≡CH(g)△H2=+32.4kJ·mol-1
则相同条件下,反应C3H8(g) CH3CH=CH2(g)+H2(g)的△H=kJ·mol-1。
CH3CH=CH2(g)+H2(g)的△H=kJ·mol-1。
(2)碳氢化合物完全燃烧生成CO2和H2O。常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10-5 mol·L-1。若忽略水的电离及H2CO3的第二级电离,则H2CO3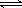 HCO3-+H+的电离平衡常数Ka1=。(已知:10-5.60=2.5×10-6)
HCO3-+H+的电离平衡常数Ka1=。(已知:10-5.60=2.5×10-6)
(3)在1 L浓度为c mol/LCH3COOH溶液中,CH3COOH分子、H+和CH3COO-离子物质的量之和为nc mol,则CH3COOH在该温度下的电离度为×100%
恒容容积为VL的密闭容器中发生2NO2 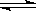 2NO+O2反应。反应过程中NO2的物质的量随时间变化的状况如图所示。
2NO+O2反应。反应过程中NO2的物质的量随时间变化的状况如图所示。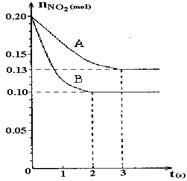
(1)若曲线A和B表示的是该反应在某不同条件下的反应状况,则该不同条件是。
A.有、无催化剂 B.温度不同
C.压强不同 D.体积不同
(2)写出该反应的化学平衡常数K的表达式:,并比较K800℃K850℃(填“>”、“<”或“=”)。
(3)求算在B条件下从反应开始至达到平衡,氧气的反应速率v(O2)=。
(4)不能说明该反应已达到平衡状态的是。
A.v正(NO2)=v逆(NO)B.c(NO2)=c(NO)
C.气体的平均摩尔质量不变D.气体的密度保持不变
若起始温度相同,分别向三个容器中充入2molNO和1molO2 ,则达到平衡时各容器中NO物质的百分含量由大到小的顺序为(填容器编号)。