下列反应的离子方程式正确的是
| A.FeCl3溶液中加入铁粉:Fe3++Fe=2Fe2+ |
| B.钠和水反应:Na+H2O =Na++OH-+H2↑ |
| C.硫酸溶液中滴加氢氧化钡溶液:Ba2++SO42-=BaSO4↓ |
| D.向烧碱溶液中滴加盐酸:OH-+H+=H2O |
在标准状况下,n L NH3溶于m mL水中,得到密度为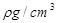 的氨水,则氨水的物质的量浓度是
的氨水,则氨水的物质的量浓度是
A.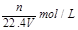 |
B.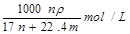 |
C.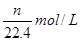 |
D.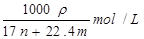 |
配制一定物质的量浓度的某溶液,下列情况会使配制结果偏高的是
| A.将溶质用蒸馏水溶解后,未冷却即转移至容量瓶中并定容 |
| B.未洗涤溶解溶质用的烧杯及玻璃棒 |
| C.定容时仰视刻度线观察液面 |
| D.容量瓶中原来含有少量蒸馏水 |
下列能达到实验目的的是
① ②
② ③
③ ④
④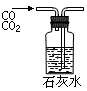
| A.①吸收氨气制氨水 | B.②制取少量蒸馏水 |
| C.③转移溶液 | D.④除去杂质气体CO2 |
在aLAl2(SO4)3和(NH4)2SO4的混合溶液中加入bmol的BaCl2,恰好使溶液中的SO42-完全沉淀;如加入足量强碱并加热可得到cmolNH3,则原溶液中的Al3+的浓度(mol/L)为
A.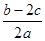 |
B. |
C. |
D. |
NA代表阿伏加德罗常数,下列叙述正确的是
| A.在H2O2+Cl2=2HCl+O2反应中,每生成32g氧气,则转移2NA个电子 |
| B.10mL质量分数为98%的H2SO4,用水稀释至100mL,H2SO4的质量分数为9.8% |
| C.一定温度下,1molFeCl3水解生成NA个Fe(OH)3胶体颗粒 |
| D.在标准状况下,2.24L苯中所含分子数约为NA |