NA代表阿伏加德罗常数,下列叙述正确的是
| A.在H2O2+Cl2=2HCl+O2反应中,每生成32g氧气,则转移2NA个电子 |
| B.10mL质量分数为98%的H2SO4,用水稀释至100mL,H2SO4的质量分数为9.8% |
| C.一定温度下,1molFeCl3水解生成NA个Fe(OH)3胶体颗粒 |
| D.在标准状况下,2.24L苯中所含分子数约为NA |
、设NA为阿伏加德罗常数的值。下列叙述正确的是( )
| A.1 mol甲醇中含有C-H键的数目为4NA |
| B.25 ℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA |
| C.标准状况下,2.24 L己烷含有分子的数目为0.1NA |
| D.常温常压下,Na2O2与足量H2O反应,共生成0.2 mol O2,转移电子的数目为0.4NA |
、下图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此,下列说法正确的是( )
| A.该硫酸的物质的量浓度为9.2mol·L-1 |
| B.1mol Zn与足量的该硫酸反应,标准状况下产生22.4L气体时,转移的电子数为NA |
| C.配制200mL 4.6mol·L-1的稀硫酸需取该硫酸50mL |
| D.该硫酸与等体积的水混合后所得溶液的物质的量浓度等于9.2mol·L-1 |
、把500 mL含有BaCl2和KCl的混合溶液分成5等份,取一份加入含amol硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含bmol硝酸银的溶液,恰好使氯离子完全沉淀。则该混合溶液中钾离子浓度为( )
| A.0.1(b-2a)mol·L-1 | B.10(2a-b)mol·L-1 |
| C.10(b-a)mol·L-1 | D.10(b-2a)mol·L-1 |
、设NA表示阿伏加德罗常数,下列说法正确的是 ()
①6.8g熔融的KHSO4中含有0.1NA个阳离子
②1L 1mol·L-1的盐酸中,含HCl分子数为NA
③常温常压下,11.2L的CH4中含有的氢原子数为2NA
④0.1mol Na2O2与水完全反应,转移0.2NA个电子
⑤62g Na2O溶于水中,所得溶液中有NA个O2-
⑥1L 1mol·L-1的醋酸溶液中离子总数为2NA
⑦标准状况下,22.4L氩气含有原子数为2NA
⑧常温常压下,32g O2、O3的混合物含有2NA个氧原子
⑨1L 1mol·L-1的酒精溶液,含有NA个分子
⑩1mol Fe和足量的盐酸反应,失去3 NA个电子
| A.②③⑤ | B.③⑥⑧ | C.①⑨ | D.⑧ |
下列叙述正确的是
| A.乙酸与丙二酸互为同系物 |
| B.不同元素的原子构成的分子只含极性共价键 |
C.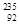 U和 U和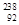 U是中子数不同质子数相同的同种核素 U是中子数不同质子数相同的同种核素 |
| D.短周期第ⅣA与ⅦA族元素的原子间构成的分子,均满足原子最外层8电子结构 |