某酸的酸式盐NaHY在水溶液中,HY—的电离程度小于HY—的水解程度,有关叙述正确的是
A.H2Y在电离时:H2Y+H2O HY—+H3O+ HY—+H3O+ |
| B.在该盐的溶液中,离子浓度为:c(Na+)>c(HY—)>c(Y2—)>c(OH—)>c(H+) |
| C.在该盐的溶液中,离子浓度为:c(Na+)>c(Y2—)>c(HY—)>c(OH—)>c(H+) |
D.HY—水解方程式为:HY—+H2O Y2—+H3O+ Y2—+H3O+ |
欲将蛋白质从水溶液中析出而又不改变蛋白质的性质,应加入的试剂是
A.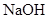 溶液 溶液 |
B.(NH4)2SO4溶液 |
| C.CuSO4溶液 | D.酒精溶液 |
有关糖类物质概念的叙述中,正确的是
| A.糖类都是具有甜味的物质 |
| B.糖类都是符合通式Cn(H2O)m的物质 |
| C.葡萄糖具有还原性,它是一种多羟基醛 |
| D.淀粉是一种白色粉末,本身有甜味 |
2008年初,中国南方的大雪引发了巨大灾难。下列说法不正确的是
| A.雪是由水蒸气凝华而成的,该过程有能量放出 |
| B.雪融化为水后能量增加 |
| C.雪融化为水时要吸收能量,导致环境温度升高 |
| D.在雪上撒大量的以NaCl、MgCl2等为主要成分的融雪剂 |
当今国际能源研究的热点之一是寻找新能源,下列能源不属于新能源的是
| A.太阳能 | B.氢能 |
| C.地热能 | D.水能 |
如下图装置(I)为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池电的化学方程式为:
(II)为电解池的示意图。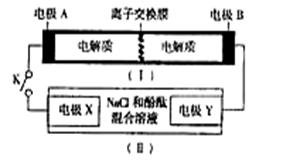
当闭合开关K时,电极X附近溶液先变红。则闭合K时,下列说法正确的是
| A.电极A上发生的反应为:2S22---2e-=S42- |
| B.K+从右到左通过离子交换膜 |
| C.电极X上发生的反应为:2Cl--2e-=Cl2↑ |
| D.当有0.1 mol K+通过离子交换膜,Y电极上产生2.24 L气体(标准状况) |