下列有关实验原理、方法和结论都正确的是:
| A.某无色溶液滴加氯水和CCl4,振荡、静置分层后,下层溶液显紫色,则原溶液中有I- |
| B.取少量溶液X,向其中加入适量新制氨水,再加几滴KSCN溶液,溶液变红, 说明X溶液中一定含有Fe2+ |
| C.向某溶液中滴加BaCl2溶液,若有白色沉淀,再滴加足量稀HNO3,若沉淀不溶解, 则说明原溶液中一定含SO42— |
| D.某无色溶液用洁净铂丝蘸取溶液进行焰色反应,火焰呈黄色,则原溶液含有Na+无K+ |
在密闭容中发生下列反应aA(g)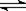 cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
| A.A的转化率增大 | B.平衡向正反应方向移动 |
| C.D的体积分数变大 | D.a < c+d |
向一体积为2L的恒容密闭容器里充入1 mol N2和4 molH2,在一定温度下发生反应: N2(g)+3H2(g) 2NH3(g);△H<0。10秒后达到平衡,c(NH3)为0.4mol/L。下列说法正确的是
2NH3(g);△H<0。10秒后达到平衡,c(NH3)为0.4mol/L。下列说法正确的是
| A.该反应达平衡时H2的转化率为40% |
| B.降低温度能使混合气体的密度增大 |
| C.向该容器中充入N2,平衡正向移动 |
| D.研发高效催化剂可大大提高N2的转化率 |
A、B、C、D四种短周期元素的原子半径依次减小,A 与C的核电荷数之比为3:4,D能分别与A、B、C形成电子总数相等的分子X、Y、Z。下列叙述正确的是
A.X、Y、Z的稳定性逐渐减弱
B.A、B、C、D只能形成5种单质
C.X、Y、Z三种化合物的熔沸点逐渐降低
D.自然界存在多种由A、B、C、D四种元素组成的化合物
下列说法中,能说明化学平衡一定向正反应方向移动的是
A.N2O4(g) 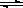 2NO2(g),改变某一条件后,气体颜色加深 2NO2(g),改变某一条件后,气体颜色加深 |
B.N2(g) + 3H2(g) 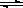 2NH3(g),改变某一条件后,NH3的体积分数增加 2NH3(g),改变某一条件后,NH3的体积分数增加 |
C.H2(g) + I2(g) 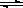 2HI(g),单位时间内消耗H2和HI的物质的量之比大于1∶2 2HI(g),单位时间内消耗H2和HI的物质的量之比大于1∶2 |
D.2SO2(g) + O2(g) 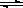 2SO3(g),恒温恒容充入He 2SO3(g),恒温恒容充入He |
下列说法中,正确的是
| A.热化学方程式中的化学计量数表示物质的量,可以是分数 |
| B.△H > 0 kJ·mol-1表示放热反应,△H < 0 kJ·mol-1表示吸热反应 |
| C.1 mol H2SO4与1 molBa(OH)2反应生成H2O时放出的热叫做中和热 |
| D.1 mol H2与0.5 molO2反应放出的热就是H2的燃烧热 |