下列排列顺序正确的是
A.常温下将0.1 mol·L-1 NH4Cl溶液与0.05 mol·L-1 NaOH溶液等体积混合,则c(Cl-)>c(Na+)>c(NH4+)>c(OH-)>c(H+)
B.常温下物质的量浓度相等的①NH4HSO4、②CH3COONH4、③NH4Cl,三种溶液中c(NH4+):①>③>②
C.0.1 mol·L-1的NaHA溶液,其pH=11,则溶液中:
c(HA-)>c(OH-)>c(A2-)>c(H2A)
D.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:
c(CH3COO-)+2c(OH-)<2c(H+)+c(CH3COOH)
三氟化氮(NF3)是一种无色、无味的气体,它是微电子工业技术的关键原料之一,可由氨气和氟气反应得到:4NH3 +3F2=NF3 +3NH4F,它在潮湿的环境中能发生反应:
3 NF3+5H2O=2NO+HNO3+9HF。下列说法正确的是( )
| A.制取NF3的反应中,氧化剂与还原剂的物质的量之比为1:3 |
| B.NF3在潮湿的空气中泄漏会产生红棕色气体 |
| C.若在制取NF3的反应中有2molNH3参加反应,转移电子的物质的量为12mol |
| D.它在潮湿的环境中NF3是氧化剂,H2O是还原剂 |
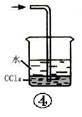
如图各装置不能达到实验目的的是( )
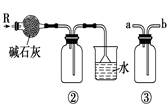
| A.装置①可制取少量蒸馏水 |
| B.装置②可用于干燥、收集氨气,并吸收多余的氨气 |
| C.装置③可用于排空气法收集NO气体 |
| D.装置④中下层物质若为四氯化碳,则可用于吸收氯化氢 |
NA表示阿伏加德罗常数。下列说法正确的是( )
| A.0.1mol Na2O2中含有的阴离子数目为0.2NA |
| B.标准状况下,2.24 L CHCl3的分子数为0.1NA |
| C.1 L 0.1 mol·L-1 Al2(SO4)3溶液中Al3+的数目为0.2NA |
| D.9.2 g NO2和N2O4的混合气体中含有的氮原子数为0.2NA |
下列盛放试剂的方法正确的是 ( )
| A.氢氟酸或浓硝酸存放在带橡胶塞的棕色玻璃瓶中 |
| B.汽油或煤油存放在带橡胶塞的棕色玻璃瓶中 |
| C.碳酸钠溶液或氢氧化钙溶液存放在配有磨口塞的棕色玻璃瓶中 |
| D.氯水或硝酸银溶液存放在配有磨口塞的棕色玻璃瓶中 |
实验表明:将氯水滴加到一张蓝色石蕊试纸上,试纸上会出现如图所示的半径慢慢扩大的内外两个圆环,且两环颜色不同,下列有关说法中不正确的是
| A.此实验表明氯水具有酸性、漂白性 |
| B.内环呈白色外环呈红色或浅红 |
| C.内外环上颜色的差异表明此变化过程中,中和反应比氧化还原反应快 |
| D.氯水中形成次氯酸的反应中还原产物是HClO |