下列反应的离子方程式正确的是
| A.石灰乳与Na2CO3溶液混合: Ca2++CO32-=CaCO3↓ |
| B.向FeI2溶液中通入过量Cl2: 2Fe2++4I-+3Cl2=2Fe3++2I2+6Cl- |
| C.氯气通入氢氧化钠溶液中: 2Cl2+2OH-=3Cl-+ClO-+H2O |
| D.钠与水的反应: Na+2H2O =Na++2OH-+H2↑ |
X、Y、Z、W为四种短周期主族元素,其中X、Z同族,Y、Z同周期,W是短周期主族元素中原子半径最大的,X原子最外层电子数是核外电子层数的3倍,Y的最高正价与最低负价代数和为6。下列说法正确的是( )
| A.Y元素最高价氧化物对应的水化物化学式H2YO4 |
| B.原子半径由大到小的顺序为:Z>Y> W |
| C.X、Z两种元素的气态氢化物中,Z的气态氢化物较稳定 |
| D.X与W形成的两种化合物中,阴、阳离子物质的量之比均为1︰2 |
下列陈述Ⅰ、Ⅱ均正确并且有因果关系的是( )
| 选项 |
陈述Ⅰ |
陈述Ⅱ |
| A |
Fe2O3是红棕色粉末 |
Fe2O3常用作红色涂料 |
| B |
SiO2是两性氧化物 |
SiO2可和HF反应 |
| C |
Al2O3难溶于水 |
Al2O3可用作耐火材料 |
| D |
SO2有氧化性 |
SO2可使溴水褪色 |
下列对金属单质及其化合物性质的描述不正确的是( )
①在金属活动顺序表中位于前面的金属均可将后面的金属从它的盐溶液中置换出来
②镁、铝、锌均是活泼金属,它们的单质在空气中均不能稳定存在
③电解Cu(NO3)2、AgNO3的混合溶液时在阳极上一定先析出银
④2Fe3++Cu =2Fe2++Cu2+,说明铜的还原性强于单质铁
⑤常温下浓硫酸几乎不与铜反应,说明浓硫酸也能使铜钝化
⑥金属元素形成的弱碱对热不稳定,受热时可以分解成相应的氧化物
| A.①②③④⑤⑥ | B.②③④⑤⑥ |
| C.①④⑤⑥ | D.①②③⑤ |
已知Cu+在酸性条件下能发生下列反应:Cu+ → Cu + Cu2+(未配平)。NH4CuSO3与足量的10mol·L-1硫酸溶液混合微热,产生下列现象:①有红色金属生成②有刺激性气味气体产生③溶液呈蓝色。据此判断下列说法一定合理的是( )
| A.气体是二氧化硫 | B.NH4CuSO3中铜元素全部被氧化 |
| C.反应后为硫酸铜溶液 | D.硫酸全部作氧化剂 |
实验宣制取少量干燥的氨气涉及下列装置,其中正确的是( )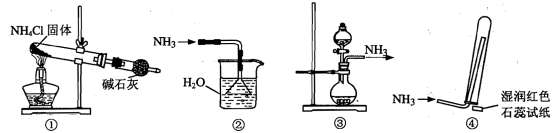
| A.①是氨气发生装置 | B.③是氮气发生装置 |
| C.②是氨气吸收装置 | D.④是氨气收集、检验装置 |