在 2Na2O2+2CO2===2Na2CO3+O2反应中,
(1)请在此方程上用双线桥法标出电子转移的方向和数目。
(2) 是还原剂, 是氧化剂。
(3)若转移3mol电子,则所产生的O2在标准状况下的体积为 ____ 。
将一定量由碳、氢、氧三种元素组成的有机化合物A的蒸气与4.8g氧气混合点燃,再将生成的气体依次通过①盛有浓硫酸的洗气瓶②饱和石灰水(设每个装置中的反应物均过量)。经测定①中增重3.60g②中增重8.80g。A蒸气的密度是相同条件下H2的38倍。又测知该有机物既能与碳酸钠溶液反应又能与金属钠反应,且均有气体生成,但得到的气体在相同条件下体积不同。试求该有机物的分子式,并写出其可能的结构简式。(写出必要的计算过程)
(10分.已知: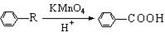 (R表示与苯环直接相连的碳原子上有氢原子的烃基)。现从A出发,发生下图所示的一系列反应,其中B和E按物质的量之比1∶2反应生成W。
(R表示与苯环直接相连的碳原子上有氢原子的烃基)。现从A出发,发生下图所示的一系列反应,其中B和E按物质的量之比1∶2反应生成W。
请回答下列问题:
(1)写出反应类型:①反应;④反应;
(2)写出W的分子式:
(3)写出下列反应的化学方程式:
②;
③。
按要求写出下列反应的方程式
(1)乙醇与氢溴酸反应_________________________________________________________
(2)甲苯硝化制TNT炸药_____________________________________________________
(3)苯酚钠溶液中通入CO2____________________________________________________
(4)乙醛与银氨溶液反应_______________________________________________________
某烃化学式为C8H10能使酸性KMnO4溶液褪色,溴水不能褪色,该烃具有_____种同分异构体,其中苯环上的一氯代物只有一种,该烃的结构简式为_________。
现有部分短周期元素的性质或原子结构如下表:
| 元素编号 |
元素性质或原子结构 |
| X |
X+具有与Ne原子相同的电子层结构 |
| Y |
最外层电子数是次外层的一半,其最高正价与最低负价的绝对值相等 |
| Z |
常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| T |
元素单质的颜色是黄绿色的气体 |
(1) Y在周期表中的位置是,Z的原子结构示意图是。
(2) X元素与T元素形成化合物的电子式是。
(3) X的最高价氧化物对应水化物的化学式是,化学键类型有。
(4) Y和Z的最高价氧化物对应的水化物中酸性较强的是(填化学式)
写出可以验证该结论的一个简单易行的实验方案
。