已知下列热化学方程式:
Zn(s)+O2(g)===ZnO(s) ΔH1=-351.1 kJ/mol
Hg(l)+O2(g)===HgO(s) ΔH2=-90.7 kJ/mol
由此可知Zn(s)+HgO(s)===ZnO(s)+Hg(l) ΔH3,其中ΔH3的值是( )
| A.-441.8 kJ/mol | B.-254.6 kJ/mol |
| C.-438.9 kJ/mol | D.-260.4 kJ/mol |
设NA为阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,11.2L HF中含有分子的数目为0.5NA |
| B.0.1molFe与少量氯气反应生成FeCl2,转移电子数为0.2NA |
| C.1.4g 由乙烯和环丙烷组成的混合物中含有原子的数目为 0.3NA |
| D.0.1 mol·L-1碳酸钠溶液中含有CO32-离子数目小于0.1 NA |
综合如图判断,下列说法正确的是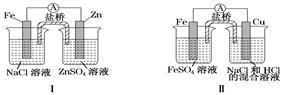
| A.装置Ⅰ和装置Ⅱ中负极反应均是Fe-2e-=Fe2+ |
| B.装置Ⅰ和装置Ⅱ中正极反应均是O2+2H2O+4e-=4OH- |
| C.装置Ⅰ和装置Ⅱ中盐桥中的阳离子均向右侧烧杯移动 |
| D.放电过程中,装置Ⅰ左侧烧杯和装置Ⅱ右侧烧杯中溶液的pH均增大 |
下列说法不正确的是
| A.Al2O3用作耐火材料、Al(OH)3用作阻燃剂 |
| B.用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 |
| C.碳素钢的主要成分是铁碳合金、司母戊鼎的主要成分是铜锡合金 |
| D.盛放NaOH溶液的磨口玻璃瓶要用橡胶塞 |
下列化合物的同分异构体数目为7种的是(不考虑立体异构)
| A.丁醇 | B.丁烯 | C.一氯戊烷 | D.己烷 |
下列实验装置不能达到实验目的的是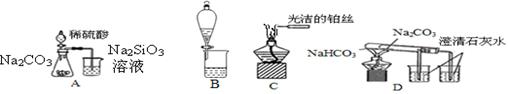
| A.比较非金属性强弱:S > C > Si |
| B.分离CH3COOC2H5和饱和碳酸钠溶液 |
| C.观察纯碱的焰色反应 |
| D.比较Na2CO3和NaHCO3的热稳定性 |