下列有关化学反应速率的说法中,正确的是
| A.铁片与稀盐酸制取氢气时,加入NaNO3固体或Na2SO4固体都不影响生成氢气的速率 |
| B.等质量的锌片分别与同体积、同物质的量浓度的盐酸、硫酸反应,反应速率不相等 |
| C.SO2的催化氧化是一个放热反应,所以升高温度,反应速率减慢 |
| D.加入反应物,反应速率常数增大,化学反应速率增大 |
若NA表示阿伏加德罗常数的值,下列说法正确的是 ( )
| A.1 mol Cl2作为氧化剂得到的电子数为NA |
| B.在0℃、101 kPa时,22.4 L氢气中含有NA个氢原子 |
| C.14 g氮气中含有7NA个电子 |
| D.NA个一氧化碳分子和0.5 mol甲烷的质量比为7∶4 |
下列叙述正确的是 ( )
A.为提醒人们在使用浓H2SO4时要注意安全,贮存浓H2SO4的容器上贴有下图标识 |
| B.实验室可通过蒸馏的方法除去自来水中含有的Cl-等杂质制蒸馏水 |
| C.做焰色反应实验时,应先将铂丝(或铁丝)用稀硫酸洗净后,在酒精灯外焰上灼烧至没有颜色时,再蘸取待检溶液进行实验 |
| D.由于碱金属单质化学性质活泼,实验室中的各种碱金属单质均保存在煤油中 |
观察下图,若用1 L水来代表地球上的总水量,要比较精确地量取地球上的淡水量,应选择的仪器是 ( )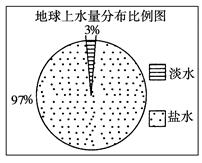
| A.100 mL烧杯 | B.50 mL烧杯 |
| C.100 mL量筒 | D.50 mL量筒 |
新型解热镇痛抗炎药扑炎痛的结构如下图所示,下列关于扑炎痛的叙述正确的是( )
| A.该物质的分子式为C17H16NO5 |
| B.该物质的核磁共振氢谱上共有9个峰 |
| C.该物质与浓溴水反应生成白色沉淀 |
| D.该物质在酸性条件下水解最终可以得到3种物质 |
食品化学家A.Saari Csallany和Christine Seppanen说,当豆油被加热到油炸温度(185 ℃)时,会产生如下图所示高毒性物质,许多疾病和这种毒物质有关,如帕金森综合症。下列关于这种有毒物质的判断不正确的是( )
A.1 mol该物质最多可以和2 mol H2发生加成反应
B.该物质的分子式为C9H15O2
C.该物质分子中含有二种官能团
D.该物质属于烃的衍生物