830K时,在密闭容器中发生下列可逆反应:
CO(g)+H2O(g) CO2(g)+H2(g)△H<0 试回答下列问题
CO2(g)+H2(g)△H<0 试回答下列问题 :
:
(1) 若起始时c(CO)="2" mol·L-1,c(H2O)="3" mol·L-1,达到平衡时CO的转化率为60%,则在此温度下,该反应的平衡常数K=
若起始时c(CO)="2" mol·L-1,c(H2O)="3" mol·L-1,达到平衡时CO的转化率为60%,则在此温度下,该反应的平衡常数K=
(2)在相同温度下,起始物质按下列四种配比充入该容器中,c(H2O)=2mol·L-1,c(CO)=c(CO2)="1" mol·L-1,c(H2)="1.5" mol·L-1,则此时该反应是否达到平衡状态 (选填“是”与“否”),此时v正 v逆(选填“大于”、“小于”或“等于”)。
(3)平衡时若降低温度,该反应的K值将 (选填“增大”、“减小”或“不变”),平衡 移动(选填“正向”、“逆向”或“不”)。
(每空2分,共10分)
研究CO2的利用对促进低碳社会的构建具有重要意义。
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等。
已知:Fe2O3(s) + 3C(石墨) =" 2Fe(s)" + 3CO(g) △H 1 =" +489.0" kJ·mol-1
C(石墨) +CO2(g) = 2CO(g) △H 2 =" +172.5" kJ·mol-1
则CO还原Fe2O3(s)的热化学方程式为。
(2)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:
CO2(g) +3H2(g) CH3OH(g) +H2O(g) △H
CH3OH(g) +H2O(g) △H
①该反应的平衡常数表达式为K=。
②取一定体积CO2和H2的混合气体(物质的量之比为1∶3),加入恒容密闭容器中,发生上述反应。反应经过相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系如图1所示,则该反应的ΔH0(填“>”、“<”或“=”)。
③在两种不同温度下发生反应,测得CH3OH的物质的量随时间变化如图2所示,曲线I、Ⅱ对应的平衡常数大小关系为KⅠKⅡ(填“>”、“<”或“=”)。
④用硫酸溶液作电解质进行电解,CO2在电极上可转化为甲烷,该电极反应的方程式为。
(共8分)
某无色溶液,其中可能存在Na+、Ba2+、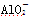 、S2-、
、S2-、 、
、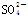 。取该溶液进行有关实验,实验结果如图所示。
。取该溶液进行有关实验,实验结果如图所示。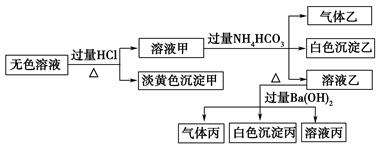
请回答下列问题:
(1)沉淀甲的化学式为________,白色沉淀乙的化学式为________
(2)由溶液甲生成沉淀乙的离子方程式为__________________。
(3)沉淀丙中一定含有_________(填化学式,下同),可能含有_______________。
(4)综合上述信息,该溶液中肯定存在的离子有_____________。
(共12分)
电化学知识是化学反应原理的重要部分,以下是常见的电化学装置:
(1)某兴趣小组同学模拟工业上用离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。
①该电解槽的阳极反应式为_______________________。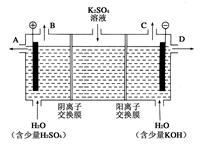
②得到的氢氧化钾从(填A,或D)排放出。常温下,若将得到的2L浓度为0.25mol/L的KOH溶液与2L0.025mol/L的硫酸溶液混合(假设溶液混合后忽略体积变化),pH为
③此时通过阴离子交换膜的离子数(填大于,小于或等于)通过阳离子交换膜的离子数。
④若将制得的氢气、氧气和硫酸溶液组合为氢氧燃料电池,则电池正极的电极反应式为____________________________________________
(2)如图所示是一套电化学实验装置,图中C、D均为铂电极,U为盐桥,G是灵敏电流计,其指针总是偏向电源正极。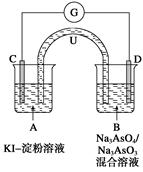
①向B杯中加入适量较浓的硫酸,发现G的指针向右偏移。此时A杯中的主要实验现象是______________________,D电极上的电极反应式为______________________。
②一段时间后,再向B杯中加入适量的质量分数为40%的氢氧化钠溶液,发现G的指针向左偏移。此时整套实验装置的总的离子方程式为__________________________。
(每空2分,共12分)
PCl3与PCl5均是有机合成的重要中间体,两者存在以下相互转化关系:
PCl5(g)  PCl3(g) + Cl2(g) △H="a" kJ·mol-1在210℃时,将4mol PCl5气体充入
PCl3(g) + Cl2(g) △H="a" kJ·mol-1在210℃时,将4mol PCl5气体充入
2L真空密闭容器中发生上述反应,得到如下数据:
| 时间(s) |
0 |
20 |
40 |
60 |
| n(PCl5) |
4 |
2.8 |
2 |
2 |
(1)已知上述反应在温度较高时才能自发进行,则a0(填﹥、﹦、﹤);
(2)计算从20s至40s共20s的时间内,用PCl3表示的平均反应速率为。210℃时该反应的平衡常数K值等于。
(3)反应进行至60s后,将混合物的温度降低,重新达到平衡后氯气浓度将(填“增大”、“减少”或“不变”)。
(4)欲增大该反应的K值,可采取的措施有(填序号)
A.降低温度 B.向混合气体中通入Cl2
C.使用高效催化剂 D.升高温度
(5)如右图是210℃时容器中PCl5物质的量的变化曲线,请在该图中补画出该反应在160℃时PCl5物质的量的变化曲线。
按要求填空,(每空2分,共6分)
双氧水(H2O2)和水都是极弱电解质,但H2O2比H2O更显酸性。
(1)若把H2O2看成是二元弱酸,请写出它在水中的电离方程式:_______________
(2)写出实验室用双氧水制取氧气的化学方程式:
(3)鉴于H2O2显弱酸性,它可以同强碱作用形成正盐,在一定条件下也可形成酸式盐。请写出H2O2与Ba(OH)2作用形成正盐的化学方程式:______________