某无色透明溶液中可能大量存在Ag+、Mg2+、Fe3+中的几种离子。
(1)不做任何实验就可以肯定原溶液中不存在的离子是 。
(2)取少量原溶液加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,白色沉淀不消失,说明原溶液中肯定有的离子 , 有关的离子反应式为 。
(3)取(2)的滤液加入过量NaOH溶液,出现白色沉淀,说明原溶液中肯定存在的离子有 。
(4)原溶液中可能大量存在的阴离子是下列A~D中的(填序号) 。
| A.Cl- | B.NO3- | C.CO32- | D.OH- |
中学化学中常见的几种物质存在下图所示的转化关系。其中,A是一种黑色粉末状固体,C是一种黄绿色气体,实验室中常用E溶液吸收多余的C。(图中部分产物和反应条件已略去)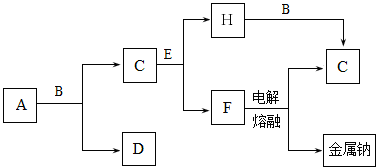
回答下列问题:
(1)写出A与B的浓溶液反应的化学方程式。
(2)固体E中含有化学键的类型是,C与E反应的离子方程式为。
(3)将B的浓溶液与H的浓溶液混合,立即产生大量气体C,该反应的离子方程式为。
(4)某课外小组的同学用E溶液吸收C,利用下图所示装置向吸收液中持续通入SO2气体。
实验过程中观察到如下现象:
①开始时,溶液上方出现白雾,试纸a变红。甲同学认为是HCl使a变红,乙同学不同意甲的观点,乙同学的认为使a变红的是(写出一种即可)。
②片刻后,溶液上方出现黄绿色气体,试纸b变蓝。用离子方程式解释b变蓝的原因。
③最终试纸b褪色。同学们认为可能的原因有两种:一是I2有还原性,黄绿色气体等物质将其氧化成
IO3-,从而使蓝色消失;二是。
X、Y、Z、W、R是短周期元素,原子序数依次增大。X原子核外各层电子数之比为1:2, Y原子和Z原子的核外电子数之和为20,W和R是同周期相邻元素,Y的氧化物和R的氧化物均能形成酸雨。
请回答下列问题:
(1)元素X的最高价氧化物的电子式为;元素Z的离子结构示意图为。
(2)单质铜和元素Y的最高价氧化物对应水化物的稀溶液发生反应的化学方程式为。
(3)元素W位于周期表的第族, 其非金属性比元素R弱,用原子结构的知识解释原
因。
(4)R的一种氧化物能使品红溶液褪色,工业上用Y的气态氢化物的水溶液做其吸收剂,写出吸收剂
与足量该氧化物反应的离子方程式。
(5)Y和Z组成的化合物ZY,被大量用于制造电子元件。工业上用Z的氧化物、X单质和Y单质在
高温下制备ZY,其中Z的氧化物和X单质的物质的量之比为1:3,则该反应的化学方程式为。
沼气(主要成分是甲烷)是一种廉价的能源,把农村中大量存在的农作物秸秆、杂草、人畜粪便等在沼气池中发酵,便可产生沼气,沼气完全燃烧可以用来点灯、做饭。
(1)在101kPa时,32gCH4燃烧生成CO2和气态H2O,放出1604kJ的热量,写出甲烷燃烧的热化学方程式为__________________________________________________________。
(2)120℃,取CH4和过量O2的混合气体共0.4mol,点燃使其充分反应,将燃烧后的气体通过足量的碱石灰(NaOH和CaO的固体混合物)充分吸收,碱石灰增重8g。计算:原混合气体中CH4和O2的体积比是多少?
某芳香烃X是一种重要的有机化工原料,质谱法测定其相对分子质量为92.现以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去),其中A是一氯代物,F的分子式为C7H7NO2,Y是一种功能高分子材料。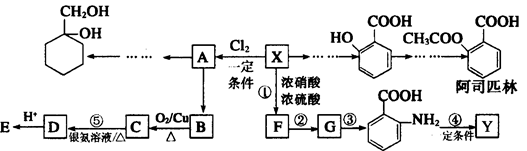
已知:
请根据所学知识与本题所给信息回答下列问题:
(1)X的化学式是_____________,其核磁共振氢谱图有____________个吸收峰;
(2)反应⑤的化学方程式是______________________________;
(3)阿司匹林分子中含有的官能团的名称是______________;1mol阿司匹林与足量NaOH溶液反应最多消耗NaOH的物质的量为_____________________。
(4)Y的结构简式为___________________________________。
(5) 有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有 _________种;
有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有 _________种;
(6)以下是由A和其它物质合成 的流程图,
的流程图,
甲→乙反应的化学方程式为_______________________________________________。
有机物A的分子式为C9H10O2,A在光照条件下生成一溴代物B,B分子的核磁共振氢谱中有4组峰,峰面积比为2:2:2:3,B可发生如下转化关系(无机产物略):
已知:①K与氯化铁溶液发生显色反应,且环上的一元取代物只有两种结构;
②当羟基与双键碳原子相连时,会发生如下转化:RCH=CHOH→RCH2CHO;
请回答下列问题:
(1)B中含氧官能团的名称是,反应①~⑤中属于取代反应的是。
(2)写出结构简式:G,E。
(3)写出下列反应的化学方程式:
反应①:,
反应③:。
(4)同时符合下列要求的K的同分异构体有种;
写出其中任意一种同分异构体的结构简式:。
Ⅰ.苯环上的一元取代物只有两种结构
Ⅱ.能发生银镜反应
Ⅲ.与氯化铁溶液发生显色反应