氨气分子空间构型是三角锥形,而甲烷是正四面体形,这是因为
| A.NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强 |
| B.NH3分子中N原子形成三个杂化轨道,CH4中C原子形成4个杂化轨道 |
| C.两种中心原子杂化轨道类型不同,NH3为sp2型杂化,而CH4是sp3型杂化 |
| D.以上说法都不正确 |
现有H2SO4、BaCl2、K2CO3、FeSO4和氯水五种溶液,有如图所示的相互反应,图中每条连线两端的物质可以发生反应。下列判断不合理的是()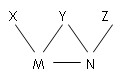
| A.X一定为H2SO4 |
| B.Y一定为K2CO3 |
| C.Z可能为氯水 |
| D.M、N必定各为BaCl2、FeSO4中的一种 |
二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示。常温下,S2Cl2是一种橙黄色的液体,遇水易水解,并产生能使品红溶液褪色的气体。下列说法中错误的是()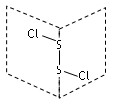
| A.S2Cl2的结构式Cl—S—S—Cl |
| B.S2Cl2的含有极性键和非极性键的非极性分子 |
| C.S2Br2与S2Cl2结构相似,熔沸点:S2Br2>S2Cl2 |
| D.S2Cl2与H2O反应的化学方程式可为2S2Cl2+2H2O═SO2↑+3S↓+4HCl |
检验某未知溶液是否含有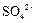 ,下列操作最合理的是()
,下列操作最合理的是()
| A.加入HNO3酸化的Ba(NO3)2溶液 |
| B.加入盐酸酸化的BaCl2溶液 |
| C.先用盐酸酸化,若有沉淀产生,过滤,在滤液中再加BaCl2溶液 |
| D.先加BaCl2溶液,若有沉淀产生,再加盐酸 |
下列反应中,调节反应物用量或浓度,不会改变反应产物的是()
| A.铁在硫蒸气中燃烧 | B.H2S在空气中燃烧 |
| C.二氧化硫通入澄清石灰水 | D.硫酸中加入锌粉 |
下列有关浓H2SO4性质的叙述中,错误的是()
| A.浓硫酸具有脱水性,因而能使蔗糖炭化 |
B.在反应HCOOH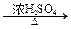 CO↑+H2O中,浓H2SO4只表现脱水性 CO↑+H2O中,浓H2SO4只表现脱水性 |
C.在反应Cu+2H2SO4(浓)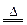 CuSO4+SO2↑+2H2O中,浓H2SO4只表现氧化性 CuSO4+SO2↑+2H2O中,浓H2SO4只表现氧化性 |
| D.浓硫酸具有吸水性,因而能使CuSO4·5H2O转化为CuSO4 |