.2009年10月16日第十一届全运会在济南举行,全运会使用的火炬的燃料是丙烷。
(1)已知11g丙烷完全燃烧生成CO2和液态水时放出的热量为555kJ,请写出丙烷燃烧热的热化学方程式
(2)某温度下,纯水中的c(H+)=2.0×10-7mol/L,若温度不变,滴入稀硫酸使c(H+)=5.0×10-6mol/L,则该溶液中由水电离出的c(OH-)为
以煤为主要原料可以制备乙二醇,相关工艺流程如下:
(1)写出方法l在催化剂的条件下直接制取乙二醇的化学方程式
(2)合成气在不同催化剂作用下,可以合成不同的物质。下列物质仅用合成气为原料就能得到且原子利用率为100%的是(填字母)。
A.草酸( HOOC-COOH)B.甲醇(CH3OH)C.尿素[CO(NH2)2]
(3)工业上还可以利用天然气(主要成份为CH4)与C02反应制备合成气。已知:
CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ/mol
2H2(g)+ O2(g)= 2H2O(l) △H=-571.6kJ/mol
2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ/mol
则CH4与CO2生成合成气的热化学方程式为。
(4)方法2:在恒容密闭容器中投入草酸二甲酯和H2发生如下反应:
CH3OOC—COOCH3(g)+ 4H2(g) HOCH2CH2OH(g)+2CH3OH(g)△H=-34kJ/mol
HOCH2CH2OH(g)+2CH3OH(g)△H=-34kJ/mol
为提高乙二醇的产量和速率,宜采用的措施是___________(填字母)。
A.升高温度B.增大压强 C.增大氢气浓度
(5)草酸二甲酯水解生成草酸:CH3OOC—COOCH3+ 2H2O HOOC—COOH+2CH3OH
HOOC—COOH+2CH3OH
①草酸是二元弱酸,可以制备 (草酸氢钾),
(草酸氢钾), 溶液呈酸性,用化学平衡原理解释:。
溶液呈酸性,用化学平衡原理解释:。
②在一定的 溶液中滴加NaOH溶液至中性。下列关系一定不正确的是(填字母)。
溶液中滴加NaOH溶液至中性。下列关系一定不正确的是(填字母)。
A.
B.
C.
(6)乙二醇、空气在KOH溶液中构成燃料电池,加入乙二醇的电极为电源的(填“正”或“负”)级,负极反应式为。
A、B、C、D、E是原子序数依次增大的短周期元素,A是短周期中金属性最强的元素,B是地壳中含量最高的金属元素,C单质的晶体是良好的半导体材料,D的最外层电子数与内层电子数之比为3:5。
(1)C的原子结构示意图为 ,D在元素周期表中的位置
(2)A单质在氧气中燃烧生成化合物甲,甲中所含化学键为;A单质在E单质中燃烧生成化合物乙,用电子式表示乙的形成过程。
(3)F是中学化学常见元素,它的一种氧化物为红棕色粉末,B单质与其在高温条件下反应是冶炼F单质的方法之一,该反应的化学方程式为。
(4)含B元素的化合物常用作净水剂,用文字和化学用语解释净水原因:。
(5)E元素的非金属性强于D元素,用原子结构解释原因:同周期元素随着原子序数的递增,,,非金属性增强。
(6)工业上将干燥的E单质通人D熔融的单质中可制得化合物D2E2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为。
有如图电解装置,图中A装置中盛1 L 2 mol· L—1AgNO3溶液,B装置中盛1L 2 mol·L—1Na2SO4溶液。通电后,湿润的KI淀粉试纸的C端变蓝色,电解一段时间后,试回答: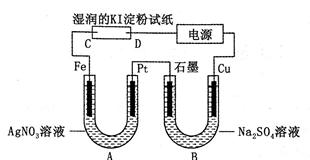
(1)A中发生反应的化学方程式为___________________________________________。
(2)在B装置中观察到的现象是____________________________________________。
(3)室温下,若从电解开始到时间为T时,A、B装置中共收集到气体0.168L(标准状况),若电解过程中无其他副反应发生,且溶液体积变化忽略不计。试计算:T时刻A装置溶液中c(H+)(写出计算过程)。
钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢材年产量的四分之一。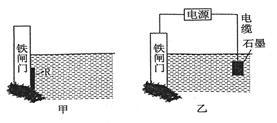
(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式为________________
(2)为了降低某铁闸门被腐蚀的速率,可以采用上述图甲所示的方案,其中焊接在铁闸门上的固定材料R可以采用____(填序号)。
| A.铜 | B.钠 | C.锌 | D.石墨 |
(3)上图乙所示的方案也可以降抵铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的_______极。
现有NH4Cl和氨水组成的混合溶液。请回答下列问题(填“>”、“<”或“=”):
(1)若溶液的pH=7,则该溶液中c(NH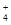 )_________c (Cl—)。
)_________c (Cl—)。
(2)若溶液的pH>7,则该溶液中c(NH+)_________c(Cl—)。
(3)若c(NH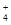 )<c (Cl—),则溶液的pH__________7。
)<c (Cl—),则溶液的pH__________7。