(4分) 甲、乙、丙三种物质均含地壳中含量最多的元素。甲、乙是组成元素相同的化合物,丙是单质;甲、乙在常温下均为液体,在一定条件下均可分解成丙;它们之间有如右图所示的转化关系(部分物质和反应条件已经略去)。则:甲的化学式为 ;丙转化成乙的化学方程式为 ;
从微观的角度解释甲、乙性质有差异的原因是 。
候德榜是我国著名的制碱专家,在改进 (填物质名称)生产方面做出了杰出的贡献,发明了联合制碱法,其原理的最后一步是:将析出的碳酸氢钠加热即制得该物质,同时生成一种生活中常见的液体和一种使澄清石灰水变浑浊的气体,请写出反应的化学方程式:
人们通常把的过程叫做结晶。结晶的方法主要有和法。法是适用于一切把可溶于水的物质从溶液中分离出来的方法;当晶体从饱和溶液中析出后,剩余的液体被称为母液,它通常是(填饱和溶液或不饱和溶液)。
饱和溶液与不饱和溶液不是绝对的,在一定的条件下可以相互进行转化。请将实现转化的方法填在横线上。
(1)由硝酸钾饱和溶液变为不饱和溶液的方法有
(2)由硝酸钾的不饱和溶液变成饱和溶液的方法有
通过近一个学期的化学学习,你已经掌握了实验室制取气体的有关规律,请结合下图回答问题: 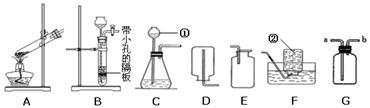
(1)写出编号所指仪器的名称:①;②;
(2)以上装置图中共有两处明显的错误,请你找出其中一处并把改正的结果填在下列横线上:;
上述装置改进后,请继续回答下列问题:
(3)扎西在实验室中用氯酸钾和另一种固体制取氧气,他选择上述装置中的(填字母)和F进行组装。小红在实验室中选用C装置作为氧气的发生装置。在他们的实验中都用到了一种相同的固体药品,在两个反应中它起作用。请你写出小红制取氧气的化学反应方程式:;
(4)实验室选用C和E装置还可以制取的气体是(填化学式),写出实验室检验该气体的方法;
(5)装置B、C都可以用来制取(4)中的气体,比较这两个装置的不同,指出B装置的一个突出优点;
(6)有一名同学欲用G装置收集H2,则H2应从导管口通入。
水是生命之源,也是人类最宝贵的资源。请回答下列问题。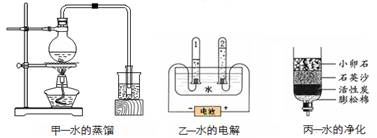
(1)自然界中的水都不是纯水,利用沉淀、、吸附和等方法可以净化水。
(2)甲中的水只发生了______(填“物理”或“化学”)变化。
(3)乙是水通电分解的示意图。在实验过程中,试管2中产生的气体名称是,
该反应的化学方程式是。
(4)丙是用来净化河水的简易装置,下面对该净水器的作用分析正确的是(填序号)。
| A.能杀菌消毒 | B.能得到纯净水 |
| C.能把硬水变为软水 | D.能使河水变得无色澄清 |