(10无锡31)有A、B、C、D四种元素,已知A元素的原子核外只有1个电子,B是地壳中含量最高
的元素,C2--离子核外有18个电子,D是血红蛋白的组成元素之一,人体缺乏该元素会引
起贫血。写出A、B、D三种元素的名称或符号;A B D ;
C2--离子的符号为 ; B、C、D三种元素组成化合物的化学式为
我国是世界上已知矿物种类比较齐全的少数国家之一,某种矿石的主要成分为
,请回答:
(1)画出氧原子的原子结构示意图,
的元素名称是;
(2)
中钙、氧元素的原子个数比为,已知由钙、碳两种元素形成的一种化合物中钙、碳元素的质量比为5:3,则该化合物的化学式是;
(3)铝制成铝锅,是利用了铝的延展性和性(填写物理性质),铝制品不易锈蚀的原因是(用化学方程式解释).
结合以下几种实验装置,回答有关问题: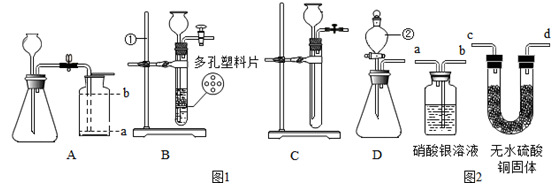
(1)写出编号仪器的名称:①,②。
(2)实验室用大理石和稀盐酸制取二氧化碳,反应的化学方程式为;用A装置制取二氧化碳,收集气体时,集气瓶中导气管口应处的位置是(选填"a"或"b"),此装置不能控制反应的发生和停止,若要随时控制反应发生或停止,应选用的装置是(填写字母)。
(3)若用如图2所示装置检验制取的二氧化碳气体中是否含有氯化氢和水蒸气, 请写出气体通过装置的接口顺序(用"a"、"b"、"c"、"d"表示)。
下图是化学兴趣小组的同学设计和改进的实验装置,请你参与他们的探究活动。回答下列问题: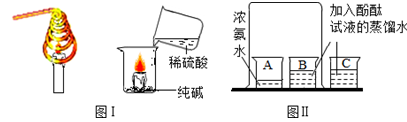
(1)图I:小明同学用一根粗铜丝绕成线圈罩在蜡烛的火焰上,火焰很快熄灭。请分析蜡烛火焰熄灭的原因,此实验说明金属铜具有性。
小娟同学在铺有一层纯碱粉末的烧杯中点燃一支蜡烛,然后沿着烧杯壁缓缓倒入稀硫酸,蜡烛火焰熄灭。请分析蜡烛熄灭的原因,写出纯碱与稀硫酸反应的化学方程式,此反应类型属于。
(2)图II:小亮同学在烧杯A中加入10
浓氨水;在烧杯B、C中都加入20
蒸馏水,并分别滴加3滴酚酞试液于蒸馏水中,得到无色溶液。用一只大烧杯把A、B两烧杯罩在一起,几分钟后,溶液颜色变成红色的烧杯是(选填"A"、"B"或者"C"),请你用分子的知识解释烧杯中溶液变红的原因;若用pH试纸测试,该溶液的pH一定(选填">"、"="或者"<")7。
请分析、比较以下几组化学反应,得出结论。
| 组别 |
化学方程式 |
结论 |
| I |
|
反应物相同,生成物不同, 原因。 |
| II |
|
反应物相同,生成物不同, 原因。 |
| III |
|
反应物相同,生成物不同, 原因。 |
| IV |
(反应缓慢) (反应迅速) |
反应物相同,反应速率不同, 原因。 |
| 实践与应用 |
科学探究正努力实现对化学反应的控制,很多化学家致力于研究二氧化碳的"组合转化"技术,把过多二氧化碳转化为有益于人类的物质。若让二氧化碳和氢气在一定条件下反应,可生成一种重要的化工原料,反应的化学方程式如下: ,推断X的化学式是。 |
溶解度曲线为定量描述物质的溶解性提供了便利。下图是甲、乙两种物质的溶解度曲线。请据图回答:
(1)t1℃时甲物质的溶解度乙物质的溶解度(选填“>”、“=”、“<”);
(2)当甲物质的溶液中含有少量乙物质时,可以采用的提纯方法是;
(3)t2℃时,将甲、乙两种物质的饱和溶液各50克,分别蒸发掉10克水,甲溶液析出晶体的质量乙溶液析出晶体的质量(选填“>”、“=”、“<”)。