实验室欲配制1000g溶质质量分数为4%的氢氧化钠溶液。请回答下列问题;
(1)配制步骤
①计算:需氢氧化钠固体 g,水960mL(水的密度是1 g/cm3)。
②称量:用质量为23.1 g的烧杯作称量容器,托盘天平上称取氢氧化钠固体时,盛有氢氧化钠固体的烧杯应放在左盘。
③溶解:将氢氧化钠固体溶于水,用玻璃棒搅拌,使氢氧化钠全部溶解,冷却至室温。
④装瓶:把配好的溶液装入试剂瓶,盖好瓶盖并贴上标签,放入试剂柜中。
请在装有所配制溶液的试剂瓶(见下图)标签上标明相应的信息。
(2)配制过程,导致溶液中氢氧化钠质量分数小于4%的可能原因是
①用量筒量取水时俯视读数;②配制溶液的烧杯用少量蒸馏水润洗;③用托盘天平称取氢氧化钠,将氢氧化钠放置在右盘;④盛装溶液的试剂瓶用蒸馏水润洗;⑤氢氧化钠固体不纯。
(3)若老师提供的药品有500 g 8%的氢氧化钠溶液,500 g 1%的氢氧化钠溶液,足量的氢氧化钠固体和水,除了上述配制方案外,你还可以设计出哪些配制方案,请你写出其中的一种: .(只要说明配制时所需的各种药品及用量即可)。
请用线段连接有对应关系的相邻两列间的点。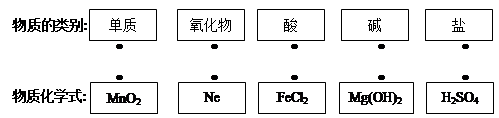
人类的生产生活离不开材料.(每空1分,计10分)
(1)人们习惯上把金、银、锡、铜、铁五种金属统称为“五金”,在“五金”顺序中把金属 的位置向左移一位,正好符合由弱到强的活动性顺序.某金属加入到稀硫酸中溶液变为浅绿色,则反应的化学方程式为。
(2)为了防止水龙头生锈,其表面常镀一层铬,其防锈的原理是:,炒菜时铁锅中的油着火可用锅盖盖灭,其原理是______________________________________。
(3)CO可作冶金工业原料,但对人体健康有害;写出高炉炼铁中CO还原氧化铁的化学反应方程式:;煤气中毒是因为CO与血液中结合,造成人体缺氧。
(4)现有一包铜、锌混合粉末,在空气中充分灼烧后,加入稀硫酸至固体恰好溶解,再加入一定量的铁粉,充分反应后过滤,得到滤渣和滤液。则滤渣中一定有;滤液中溶质一定有。
(5)家用空调常用铜线圈,这是利用铜具有优良的性,要验证镁、铝、铜的活动性顺序,他选择了打磨过的铝丝、硫酸铜溶液,你认为他还需要的溶液是______ ______溶液。
根据如图所示装置,回答下列问题.(每空1分,计10分)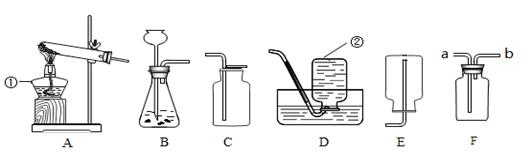
(1)标有“①”的仪器名称是,它的火焰温度最低的部分是;当②中充满氧气做硫粉在其中燃烧的实验时常在它的底部加一些水作用是 。
(2)实验室用A装置制取氧气,试管中为混合物,则发生反应的化学方程式为;已知过氧化钠粉末与水反应生成氢氧化钠和氧气,则用此法制取并收集干燥的氧气时应选用的装置组合是(填字母标号)。
(3)B装置可用来制取二氧化碳,现实验室无稀盐酸只有稀硝酸与石灰石,则反应的化学方程式为 ,实验前需检查B的气密性,方法是 。
(4)B装置也可用锌和稀硫酸来制取氢气,反应的方程式为,收集较为干燥的氢气宜选用(填字母标号),F装置可用来作排水法测氢气的体积,此时气体应从 (填a或b)口进入。
请完成下列空格:(每空1分,计10分)
(1)现有下列微粒:①NH4+ ②CuSO4 ③S8 ④SO42-⑤Ca(OH)2。其中能表示盐的是(填序号,下同),其中能表示分子的是。①和④两种微粒构成的化合物化学式,能用来检验二氧化碳的是 的溶液。
化学用语可准确、简洁表达化学信息。请用化学符号填空。
①地壳中含量具第二位的非金属元素 ②镁原子结构示意图
③ 生石灰中钙显+2价 ④最简单的有机物
⑤ 常温下呈液态的金属 ⑥n个碳酸根离子
如下图是实验室制取气体的常用仪器。请根据要求填空: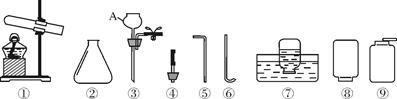
(1)图中仪器名称是②____________,
(2)小宝同学用氯酸钾和二氧化锰制取并收集一瓶氧气,应选择上图中的仪器____________(填序号,以下同),
(3)小茹同学用锌和稀硫酸制取H2,同时生成硫酸锌,则应选择上图中____________装置.
(4)小佳同学查阅资料得到制取硫化氢气体的如下信息,请回答下列问题:
| 气体 |
实验药品 |
反应条件 |
气体物理性质 |
| H2S |
硫化亚铁固体与稀硫酸 |
不需加热 |
无色,密度比空气大,可溶于水 |
制取硫化氢____________(填“可以”或“不可以”)采用装置①,理由是