实验题
Ⅰ以下是有关SO2、Cl2的性质实验。
(1)某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究SO2和Cl2的性质。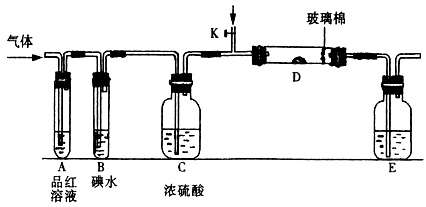
若从左端分别通入SO2和Cl2,装置A中观察到的现象是否相同? (填“相同”或“不相同”);若装置D中装的是V2O5(催化剂),通入SO2时,打开K通入适量O2的化学反应方程式为 。
②SO2通入B中,溶液颜色退去,则该反应的离子方程式为 。
(2) 某同学将足量的SO2通入一支装有氯化钡溶液的试管,未见沉淀生成,若向该试管中加入足量(填字母) ,仍然无法观察到沉淀产生。
A.氨水 B.稀盐酸 C.硝酸钾溶液 D.硫化钠溶液
(3)若由元素S和O组成–2价酸根离子X,X中S和O的质量比为2∶3;当Cl2与含X的溶液完全反应后,得澄清溶液,取少量该溶液加入盐酸酸化的氯化钡溶液,有白色沉淀产生。写出Cl2与含X的溶液反应的离子方程式 。
(4)某科研单位利用电化学原理用SO2来制备硫酸,装置如图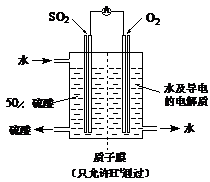
含有某种催化剂,电极为多孔的材料,能吸附气体,同时也能使气体与电解质溶液充分接触。通入SO2的电极为_________极,其电极反应式为 ;电池的总反应式
Ⅱ实验是化学研究的基础,关于下列各装置图的叙述正确的是 (填序号)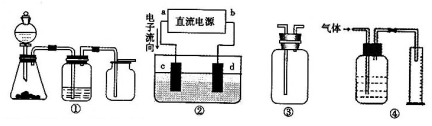
A.装置①可完成多种气体的发生、净化和收集,如铜屑与稀硝酸反应
B.装置②中,a为正极,d为阳极
C.装置③可用于收集H2、NH3、Cl2,、HCl、NO2等
D.装置④能用于测量气体体积
Ⅲ 用铅蓄电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极)。下列说法中正确的是 (填序号)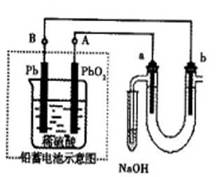
A.铅蓄电池负极的反应式为:Pb—2e-=Pb2+
B.铅蓄电池放电时,B极质量减轻,A极质量增加
C.铅蓄电池充电时,A极应与外电源负极相连
D.电解苦卤水时,a电极首先放电的是Br-
某校化学兴趣小组用浓盐酸与二氧化锰加热反应来制取并收集氯气,装置如图4-3所示。
图4-3
(1)写出该反应的化学方程式: 。
(2)上述反应中,还原剂是 ,若有1 mol氧化剂参加反应,转移的电子的物质的量是 mol。
(3)实验开始前,某学生对装置进行了气密性检查。方法:连接好装置后,用弹簧夹夹
住 (填“A”或“B”)处橡皮管;向分液漏斗中加水并打开活塞,当加到一定量时,停止加水,静置观察,当观察到分液漏斗中 时,表明该装置不漏气。
(4)兴趣小组的某些同学准备在烧杯中加入下列溶液中的一种来吸收残余氯气,你认为其中错误的是(填序号) 。
A.氢氧化钠溶液
B.碳酸钠浓溶液
C.浓硫酸
用滴管将新制的饱和氯水慢慢滴入含酚酞的NaOH稀溶液中,当滴到最后一滴时红色突然褪去。试完成下列问题:
(1)产生上述现象的原因可能有两种,请用简要的文字说明:
①____________________________________________。
②____________________________________________。
(2)简述怎样用实验证明红色褪去的原因是①还是②:______________________________。
实验室用浓盐酸、MnO2共热制Cl2,并用Cl2和Ca(OH)2反应制少量漂白粉,现已知反应:2Cl2+2Ca(OH)2====Ca(ClO)2+CaCl2+2H2O,温度稍高即发生副反应:6Cl2+6Ca(OH)2
Ca(ClO3)2+5CaCl2+6H2O。现有三个同学分别设计的三套实验装置如图所示: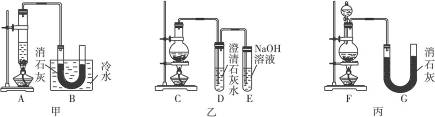
(1)a.不容易控制反应速率,b.容易控制反应速率,c.有副反应发生,d.可防止副反应发生,e.污染环境,f.可防止污染环境,请从这几个方面对上述甲、乙、丙三套装置的优缺点作出评析,并选择符合题目要求的选项填在空格内。
| 优点 |
缺点 |
|
| 甲装置 |
||
| 乙装置 |
||
| 丙装置 |
(2)上述装置中,甲由A、B两部分组成,乙由C、D、E三部分组成,丙由F、G两部分组成,请从上述装置中,选取合理的组成部分,组装一套较完善的实验装置,装置各部分的连接顺序(按气流从左到右的方向)是__________________。
(3)实验室中若用12 mol·L-1的浓盐酸100 mL与足量的MnO2反应,最终生成Ca(ClO)2的物质的量总是__________0.15 mol(填“大于”“小于”或“等于”),其原因是(假定各步反应均无反应物损耗,且无副反应发生)________________________。
实验室里化学试剂的保存方法是不相同的,下图中A、B、C、D是常见的一些保存药品的试剂瓶。请把下列常见试剂的序号填写在各试剂瓶下面的括号内:①浓硫酸②碳酸钠溶液③大理石④酒精⑤氯水⑥浓硝酸
| A |
B |
C |
D |
 |
 |
 |
 |
| () |
() |
() |
() |
A、B为两种单质,常温下均是固体。在元素周期表中A、B为前18号元素中的两种。分别取三份质量为1.52 g的A、B的混合物(粉末)进行如下实验。(本题中所有的气体体积均指标准状况下的体积)
(a)向第一份试样中加入过量的盐酸,充分反应后放出0.896 L气体,还余下0.56 g残渣;
(b)向第二份试样中加入过量的10%的NaOH溶液,充分反应后放出0.896 L气体,还余下0.96 g残渣;
(c)将第三份试样隔绝空气加强热后,生成一种固体,冷却后再加入足量的盐酸,该固体全部溶解,产生x L气体。
(1)单质A是__________。
(2)混合物中的B的质量分数是__________。
(3)写出实验(c)中有关反应的化学方程式并计算x的值。