A、B为两种单质,常温下均是固体。在元素周期表中A、B为前18号元素中的两种。分别取三份质量为1.52 g的A、B的混合物(粉末)进行如下实验。(本题中所有的气体体积均指标准状况下的体积)
(a)向第一份试样中加入过量的盐酸,充分反应后放出0.896 L气体,还余下0.56 g残渣;
(b)向第二份试样中加入过量的10%的NaOH溶液,充分反应后放出0.896 L气体,还余下0.96 g残渣;
(c)将第三份试样隔绝空气加强热后,生成一种固体,冷却后再加入足量的盐酸,该固体全部溶解,产生x L气体。
(1)单质A是__________。
(2)混合物中的B的质量分数是__________。
(3)写出实验(c)中有关反应的化学方程式并计算x的值。
(12分)某科研小组在900℃的空气中合成出化学式为La2Ca2MnOx的超导体材料,其中La以+3价存在。为确定x的值,进行如下分析:
步骤1:准确称取0.5250g超导体材料样品,放入锥形瓶中,加25.00mL0.06000mol·L-1 Na2C2O4溶液(过量)和25mL 6mol·L-1 HNO3溶液,在6070℃下充分摇动,约半小时后得到无色透明溶液A(该条件下,只有Mn元素被还原为Mn2+,Na2C2O4被氧化为CO2)。
步骤2:用0.02000mol·L-1 KMnO4溶液滴定溶液A至终点,消耗10.00mL KMnO4溶液。
(1)步骤1反应后溶液中Mn2+的物质的量浓度为0.02000mol·L-1。常温下,为防止Mn2+形成Mn(OH)2沉淀,溶液的pH的范围为[已知Mn(OH)2的Ksp=2.0×10-13]。
(2)步骤2滴定终点的现象是。
(3)步骤2滴定终点读数时俯视刻度,其他操作都正确,则所测x的值将(填“偏大”、“偏小”或“不变”)。
(4)求x的值(写出计算过程)。
(12分)聚合硫酸铁铝(PFAS)是一种新型高效水处理剂。利用硫铁矿烧渣(主要成分为Fe3O4、FeO、SiO2等)为铁源、粉煤灰(主要成分为Al2O3、Fe2O3、FeO等)为铝源,制备PFAS的工艺流程如下:
(1)“碱溶”时,Al2O3发生反应的化学方程式为。
(2)“酸溶Ⅱ”时,Fe3O4发生反应的离子方程式为。
(3)“滤渣Ⅰ”、“滤渣Ⅱ”在本流程中能加以利用的是。
(4)“氧化”时应控制温度不超过57℃,其原因是。
(5)“氧化”时若用MnO2代替H2O2,发生反应的离子方程式是。
(6)酸度对絮凝效果和水质有显著影响。若产品PFAS中残留硫酸过多,使用时产生的不良后果是。
磷酸二氢钾(KH2PO4)在工业、农业、医药及食品等行业均有广泛的应用,有报道一种湿法磷酸萃取制备磷酸二氢钾的工艺流程如下图所示(部分流程步骤已省略):
已知萃取的主要反应原理:KCl+H3PO4 KH2PO4+HCl;
KH2PO4+HCl;
HCl+E(表示有机萃取剂) HCl•E;
HCl•E;
请回答下列问题:
(1)在实验室实现流程图中操作X需要的主要玻璃仪器是 ;流程图中物质A是 ;
(2)副产品B的化学式是 ;一系列操作Y,具体包括 、洗涤、干燥;
(3)评价该工艺的优点 、 (任写两点);
(4)若用1000kg质量分数为56%的磷酸溶液,产率为98%,则可生产KH2PO4的质量为: kg;
(5)萃取一步是该流程的核心操作,萃取率、杂质脱除率受众多因素影响,请从下图中寻找出投料比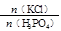 对萃取率和杂质脱除率影响的主要规律或结论(任写两条):
对萃取率和杂质脱除率影响的主要规律或结论(任写两条):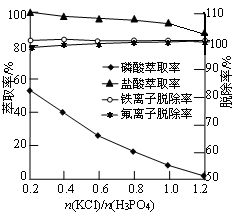
① ;
② 。
有关含氮化合物的性质实验
(一)某研究性学习小组利用图一装置研究硝酸的性质。实验一、甲同学用下图一装置来证实稀硝酸与铜反应生成NO。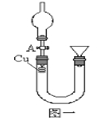
(1)从A中向U形管中注满稀硝酸后,发生的现象。
(2)以下收集NO气体的各种装置中,合理的是。(填序号,多选不给分)
(3)在100 mL 混合溶液中, HNO3和 H2SO4的物质的量浓度分别是 0.4 mol/L, 0.1 mol/L 向该混合液中加入1.92 g铜粉,加热待充分反应后,所得溶液中 Cu2+的物质的量浓度是。
实验二、乙组同学利用上述装置完成浓硝酸与铜的反应
(4)乙组同学发现实验室里有几瓶浓硝酸呈黄色,请用化学方程式和简单的文字说明解释这种现象。
(5)同学们发现反应后的溶液呈绿色,而不显蓝色。甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了NO2气体所致。同学们分别设计了以下4个实验来判断两种看法是否正确。
这些方案中可行的是。(填序号,多选不给分)
①加热该绿色溶液,观察颜色变化
②加水稀释绿色溶液,观察颜色变化
③向该绿色溶液中通入氮气,观察颜色变化
④向饱和硝酸铜溶液中通入NO2气体,观察颜色变化
(二)甲、乙、丙三位同学分别用如下三套实验装置及化学药品(其中碱石灰为固体氢氧化钠和生石灰的混合物)制取氨气。请你参与探究,并回答下列问题:
(6)写出三位同学实验装置制取氨气原理的化学方程式:。
(7)检验氨气是否收集满的方法是(简述操作方法、现象和结论)。
某校化学研究性学习小组设计如下实验方案,测定NaHCO3和Na2CO3混合物中NaHCO3的质量分数。
方案一:按下图装置进行实验。并回答以下问题。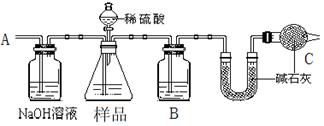
①按图组装仪器并检查装置的气密性。
②实验前称取17.90g样品,从分液漏斗滴入6mol·L-1的硫酸,直到不再产生气体时为止, 从导管A处缓缓鼓入一定量的空气。
③实验结束后测得U型管增重 8.80g。
(1)B瓶中装的试剂为______,C装置的作用是。
(2)从导管A处缓缓鼓入一定量的空气的目的是。
(3)该样品中NaHCO3的质量分数为。
方案二:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量Ba(OH)2溶液。过滤洗涤,干燥沉淀,称量固体质量,进行有关计算。
请回答:实验中判断沉淀是否完全的方法是。