a、b、c、d、e分别是Cu、Ag、Fe、Al、Mg五种金属中的一种。已知(1)a、c均能与稀硫酸反应产生氢气;(2)b和d的硝酸盐反应,置换出d单质;(3)c与强碱溶液反应放出气体;(4)c、e在冷浓硝酸中发生钝化。由此可判断a、b、c、d、e依次是
| A.Fe、Cu、Al、Ag、Mg | B.Mg、Cu、Al、Ag、Fe |
| C.Al、Cu、Ag、Mg、Fe | D.Mg、Ag、Al、Cu、Fe |
下列离子反应方程式中,书写正确的是
| A.明矾溶液加入偏铝酸钠溶液:Al3++3AlO2-+6H2O=4Al(OH)3↓ |
| B.氯化铁溶液与适量铜粉混合:Cu + Fe3+ = Cu2++ Fe2+ |
| C.Fe3O4固体溶于足量稀硝酸溶液中:Fe3O4+8H+=2Fe3++ Fe2++ 4H2O |
| D.碳酸氢铵溶液与足量澄清石灰水混合:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O |
下列根据实验操作和现象所得出的结论正确的是
| 选项 |
实验操作 |
实验现象 |
结 论 |
| A |
用铂丝蘸取溶液进行焰色反应 |
火焰呈黄色 |
溶液中无K+ |
| B |
向溶液中先滴加稀盐酸,再滴加BaCl2溶液 |
先滴加稀盐酸无现象,滴加BaCl2后出现白色沉淀 |
溶液中一定含有SO42- |
| C |
向一定浓度的CuSO4溶液中通入适量H2S气体 |
出现黑色沉淀 |
H2S的酸性比H2SO4强 |
| D |
向某溶液中滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口 |
试纸不变蓝 |
原溶液中无 |
设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.1 molCl2与足量Fe反应转移电子数一定为3NA |
| B.标准状况下,2.24 L NH3中含有共价键的数目为NA |
| C.1 mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3 NA |
| D.标况下,11.2 L SO3所含的分子数目为0.5NA |
下列各组离子在给定条件下一定能大量共存的是
| A.水电离出的c(H+)=1×10-14 mol/L的溶液:K+、[Ag(NH3)2]+、Br-、Cl- |
| B.在含有Al3+、Cl-的溶液中:HCO3-、I-、NH4+、Mg2+ |
| C.在c(H+)=1×10-13 mol·L-1的溶液中:Na+、S2-、SO32-、NO3- |
| D.在溶质为KNO3和NaHSO4的溶液中:Fe2+、Ca2+、Al3+、Cl- |
下列有关化学用语表示正确的是
A.对硝基甲苯的结构简式: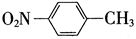 |
B.镁离子的结构示意图: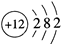 |
C.次氯酸的电子式: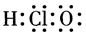 |
D.亚硫酸钠水解的离子方程式:SO32- +2H2O H2SO3+2OH- H2SO3+2OH- |