细心的同学发现在加热硫酸铜晶体时,会闻到刺激性气味,这引起了同学们的兴趣。难道生成的硫酸铜粉末受热后还能分解?那分解的产物是什么呢?
通过查阅资料,同学们了解到:
1、硫酸铜受热分解生成氧化铜和气体。气体是由SO2、SO3、O2中的一种或几种。受热时
温度不同,生成的气体成分也不同。
2、SO2、SO3都能被碱石灰吸收。
3、SO2、SO3都能被氢氧化钠溶液吸收。
【提出猜想】根据质量守恒定律猜测气体的成分:
I. 只含 ▲ 一种; II.含有SO2、O2二种; III.含有SO2、SO3、O2三种。
【设计实验】利用下图装置加热硫酸铜粉末直至完全分解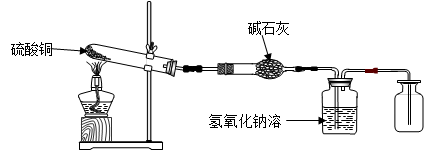
A B C D
【获取事实】
(1)用带火星的木条伸入集气瓶D,发现木条能复燃,说明气体中含有 ▲ 。
(2)已知硫酸铜粉末质量为10.0克,完全分解后,各装置的质量变化关系如下表所示:
| 装置 |
A(试管+粉末) |
B |
C |
| 反应前 |
42.0克 |
75.0克 |
140.0克 |
| 反应后 |
37.0克 |
79.5克 |
140.0克 |
请通过计算,推断出该实验条件下硫酸铜分解的化学方程式是哪一个 ? ▲
A.3CuSO4△3CuO+SO3↑+2SO2↑+O2↑ B. 4CuSO4△4CuO+2SO3↑+2SO2↑+O2↑
C.5CuSO4△5CuO+SO3↑+4SO2↑+2O2 ↑ D. 6CuSO4△6CuO+4SO3↑+2SO2↑+O2↑
请根据如图回答相关问题
(1)A中倾倒液体的操作是:取下瓶塞,倒放在桌面上,标签朝向手心,量筒稍倾斜,量筒口与 ,缓缓地向量筒中倒入液体;B中液体的体积是 mL。
(2)①小萌欲用如图C装置制气体,发现该装置中存在 处错误,小萌纠正了其中的错误,并采用向下排空气法,制取了氢气,实验室制取氢气的化学方程式为 。
②小萌又选用了不同的化学药品,用纠正错误后的C装置制得了另一种气体,该气体需用向上排空气法收集,则实验室制取该气体的化学方程式为 。
③为确定气体发生装置,应考虑反应条件和 。

松花皮蛋是黄石八珍之一。腌制皮置的一种原料是由NaCl、CaO和Na 2CO 3组成的固体混合物。某化学兴趣小组用该原料,在实验室进行如下实验:将该固体混合物放入烧杯中,加入足量的蒸馏水。充分溶解后过滤,得到白色沉淀和无色澄清滤液。同学们对滤液的溶质成分进行了探究。
请完成以下探究过程,并将①~⑤处答案填入答题卡相应位置。
固体溶解过程中发生了两个化学反应:CaO+H 2O=Ca(OH) 2 。
【提出问题】滤液中的溶质成分是什么?
【作出猜想】Ⅰ.溶质为:NaCl、NaOH、Ca(OH) 2;
Ⅱ.溶质为:NaCl、NaOH;
Ⅲ.溶质为: 。
【设计方案】
|
实验操作 |
现象 |
结论 |
|
取少量滤液于试管中,向其中滴加碳酸钠溶液 |
|
猜想Ⅰ正确 |
|
另取少量滤液于试管中,向其中滴加足量的 溶液。(填化学式) |
有气泡产生 |
猜想Ⅲ正确 |
【交流反思】兴趣小组经过讨论认为:
若猜想II正确,该原料中CaO与Na 2CO 3的质量比为 。
某学校化学兴趣小组同学在实验室发现一瓶忘了盖瓶盖的NaOH固体,对其成分是否变质以及变质程度产生了兴趣.同学们作出了以下猜想,并进行如下实验探究.
【提出问题】这瓶NaOH固体样品的成分是什么呢?
【作出猜想】猜想1:只含NaOH 猜想2:只含Na 2CO 3 猜想3:含有NaOH和Na 2CO 3
【讨论交流】NaOH可能变质的原因是 (用化学方程式表示)
【实验探究】(1)取少量样品于试管中,加入足量稀盐酸,有气泡产生,说明猜想 不成立.
(2)进一步他探究过程如下:

根据上述探究过程回答:
①加入过量BaCl 2溶液的作用是 ;
②不能用适量Ba(OH) 2溶液代替过量的BaCl 2溶液的原因是 ;
③下列溶液可用来代替酚酞试液检验猜想3成立的是 .
| A. |
CuCl 2溶液 |
B. |
KNO 3溶液 |
C. |
CaCl 2溶液 |
D. |
NH 4Cl溶液 |
【实验反思】实验室里,NaOH固体的保存方法是 .
向盛有氢氧化钠溶液的烧杯中滴加稀盐酸,搅拌后没有观察到明显现象.教材上借助酸碱指示剂验证了该反应的发生.是否还有其他方法判断该反应的发生呢?小明和小亮两位同学分别进行了实验探究.
【实验探究一】小明同学取上述反应后的溶液少许于试管中,向其中滴加硝酸银溶液,观察到有白色沉淀生成,再滴加足量的稀硝酸,沉淀不溶解.小明认为白色沉淀是NaCl与AgNO 3反应生成的,于是得出氢氧化钠与盐酸发生了反应的结论.
【实验探究二】小亮同学取一定量的稀盐酸于烧杯中,向其中逐滴加入氢氧化钠溶液,搅拌并用pH计精确测量烧杯中溶液的pH,绘制溶液的pH随时间变化的曲线如图1所示.小亮根据溶液pH的变化,推断盐酸与氢氧化钠发生了反应.

【讨论交流】(1)针对两位同学的实验探究,老师认为小明同学的结论是错误的,理由是 (用化学方程式表示).
(2)在小亮的实验中,当实验进行到10秒时,溶液中含有的溶质是 (填化学式),该溶液能与下列物质发生反应的是 (填序号).
①碳酸钠②氧化铜③硫酸铜 ④镁
(3)从图1的曲线中得知,当实验进行到 秒时,酸与碱恰好完全反应.
【拓展延伸】老师将氢氧化钠溶液逐滴加入到盛有稀盐酸的烧杯中,测定溶液的温度,绘制出溶液的温度随氢氧化钠溶液体积的变化而变化的曲线如图2所示,从能量变化的角度看,该反应属于 反应(填"吸热"、"放热").
【反思评价】有的中和反应没有明显现象,有的中和反应有沉淀生成或固体物质溶解的现象.请写出一个有沉淀生成的中和反应的化学方程式 .
矿物资源的综合利用,可以节约资源与能源.黄铁矿的主要成分为二硫化亚铁(FeS 2),黄铁矿煅烧的化学方程式:4FeS 2+11O 2═2Fe 2O 3+8SO 2.产生的SO 2用于生产硫酸,矿渣(含有少量的硫元素)用于冶铁.
查阅资料:SO 2气体能使品红溶液褪色,能使澄清石灰水变浑浊,反应的化学方程式为SO 2+Ca(OH) 2═CaSO 3↓+H 2O.
(1)FeS 2中硫元素的化合价为 .矿渣在炼铁高炉内反应产生的高炉气含CO、CO 2、SO 2等气体,其中 是形成酸雨的气体.
(2)某化学兴趣小组为检验高炉气中的CO、CO 2、SO 2,设计了如图所示装置(不考虑其他气体对该实验的影响).

①该装置不能检验出的气体是 .
②装置B的作用是 .
③装置E中发生反应的化学方程式为 .
④确认高炉气中含CO的依据是 (填小写字母).
a.装置C中澄清石灰水变浑浊 b.装置C中澄清石灰水不变浑浊
c.装置E中黑色粉末变成红色 d.装置F中澄清石灰水变浑浊
(3)请指出该装置存在的一处明显缺陷 .