小华同学用排水法收集了一大瓶沼气池中气体(图1中的A),为了弄清它的成分,进行了有关实验。请你与他一起完成以下探究活动:
【对气体猜想】猜想I:全部是CH4; 猜想Ⅱ:全部是CO;
猜想Ⅲ:是CO和CO2的混合气体; 猜想Ⅳ:是CH4和CO2的混合气体。
【实验和推断】将A中的气体依次通入B、C中,在D处点燃。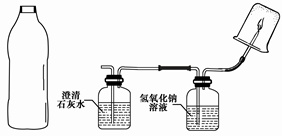

A B C D ① ② ③
图1 图2
(1)要将A中的气体通入后面的装置中,应选图2中的 (填序号)“注水装置”。
(2)若B中石灰水变浑浊,则说明A中的气体中含有 气体。
(3)装置C作用是 。
(4)若D处倒扣的是涂有澄清石灰水的烧杯,出现浑浊,且B中无明显现象,则“猜想 ”可能成立;若D处倒扣的是干冷的大烧杯,杯壁有水雾出现,有同学认为“猜想I、Ⅳ”可能成立,另有同学认为此现象不能证明收集到的气体中一定含有CH4,理由是
;要排除这种干扰可采取的措施是
。
(5)采取(4)中的排除干扰措施后:若D处分别倒扣干冷的烧杯和涂石灰水的烧杯,分别出现水雾和浑浊,且B中也出现浑浊,则证明“猜想 ”成立。
(1)目前世界上一半以上的铜用于电力和电信工业,是因为铜具有(填字母)
| A.导热性 | B.延展性 | C.导电性 | D.金属光泽 |
(2)我国第四套人民币的硬币从1999年开始发行,一元为钢芯镀镍(Ni ),五角币为钢芯镀铜合金,一角币为铝合金或不锈钢。在选择铸造硬币的材料时需要考虑的因素是有(填一条即可)。
①镍能与盐酸或稀硫酸反应,生成可溶于水的正二价镍的化合物,并放出氢气。其反应没有铁与酸反应剧烈。镍与盐酸反应的化学方程式为.
②用镍片、硫酸亚铁溶液和溶液做实验也能判断Ni 、Fe、Cu的金属活动性顺序。三种金属的活动性顺序为。
(3)若将一定质量的Zn放入CuCl2和MgCl2的混合溶液中,充分反应后过滤,所得滤液中一定含有的溶质是。
(4)活动课上小明将一枚五角币放在酒精灯火焰上加热片刻,发现表面变黑。
【假设与预测】假设Ⅰ:五角币加热变黑,是因为酒精灯内焰的黑烟附着在五角币的镀铜上;
假设Ⅱ:五角币加热变黑,是因为五角币上的镀铜与 ______发生了化学反应。
【实验与事实】
实验一: 用洁净的干布擦一擦五角币上的黑色物质,黑色物质不易被擦去;再另取一枚五角币放在石棉网上,用酒精灯加热片刻,五角币也变黑。
实验二:取一块铜片放入小试管中并塞上橡皮塞,然后用酒精灯加热直至试管中铜片变黑;再将铜片反转到另一面,加热片刻,铜片不再变黑。
【解释与结论】上述实验一和实验二证实,假设 __ ___不成立。
【表达与交流】铜片在空气中加热,发生的化学反应方程式为___ ___。
6月5日是“世界环境日”,2013年中国主题为“同呼吸共奋斗”。
(1)化石燃料是不可再生能源,包括煤、 和天然气等。
(2)下列不属于空气污染物的是 。
| A.二氧化氮 | B.二氧化硫 | C.PM2.5 | D.氧气 |
(3)二氧化碳是一种温室气体。某化学兴趣小组进行如下组合实验,对二氧化碳的性质进行验证。
当打开分液漏斗活塞后,A中出现大量气泡,B中白磷燃烧,C中液面下降,稀盐酸逐渐进入D中。E处紫色石蕊溶液变成红色,F处澄清石灰水变浑浊。
①A中发生反应的化学方程式为 。
②B中白磷能够燃烧的原因是 。
③G烧杯中 (填“上层”或“下层”)的蜡烛先熄灭,说明二氧化碳具有的物理性质是 ,具有的化学性质是 。
④E处使紫色石蕊变成红色的物质是 ;写出F处发生变化的化学方程式 。
某化学兴趣小组的同学对一瓶久置的熟石灰粉末的组成进行实验探究,请你一起参与他们的探究活动。
[提出问题]这瓶熟石灰粉末是否已经变质生成了CaCO3?
[进行猜想]猜想一: 。
猜想二:熟石灰部分变成了CaCO3。
猜想三:熟石灰没有变质。
[设计实验]该小组同学对猜想一设计了下列探究方案,请你帮助他们完成下表中相关实验内容。
| 实验步骤 |
实验现象 |
实验结论 |
| ①取样,加适量水,搅拌,过滤 ②取少量滤液于试管中,滴入酚酞试液 ③取少量滤渣于试管中,加入盐酸 |
②无明显变化。 ③。 |
猜想一成立 |
[反思与应用]①要证明猜想二成立,可参照上述实验方案进行探究,在步骤②中产生的实验现象是。
②熟石灰变质的化学反应方程式为,因此实验室中应保存。
[数据处理]将10g已经全部变质的熟石灰粉末(即CaCO3)放入烧杯中,加入一定量的稀盐酸,恰好完全反应,产生气体,完全反应后所得溶液质量为55.6g。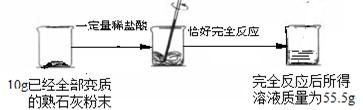
计算:①生成气体的质量为g ;参与反应的HCl的质量为g;
②反应前稀盐酸中溶质的质量分数。(写出计算过程,结果精确到0.1%)
某化学探究小组为了验证铁、铜、锌、银的金属活动性顺序,设计了如下实验方案:
①将铁片加入到稀盐酸中;
②将铜片加入到硝酸银溶液中;
③将锌片加入到稀盐酸中;
④将金属片X加入到Y中.
(该方案中所有金属均已打磨,且形状、大小以及稀盐酸的溶质质量分数均相同)
(1)写出①中反应的化学方程式: ;
(2)通过上述实验,可以判断锌的金属活动性比铁强,依据的现象是 ;
(3)要得出这四种金属的活动性顺序,如果④中Y表示硫酸铜溶液,则X表示的一种金属是;如果X表示铜,则Y表示的一种溶液是。
I.地铁站里氧气含量的测定
地铁站里氧气的含量应与地面保持一致。现有一瓶从地铁站里收集到的空气样品,康康利用下图实验装置测定样品中氧气的含量。请指出测定时需要注意的事项。(至少3条)
Ⅱ,铁的冶炼
地铁的修建需要大量的钢材。康康用下图装置模拟炼铁的化学原理,请写出反应的化学方程式。为了提高CO的利用率,你将怎样改进此装置?
Ⅲ.金属材料在地铁方面的应用
在地铁修建过程中使用了大量的金属材料
(1)地铁入口处的雨篷骨架用铝合金而不用纯铁的原因是 。
(2)钢轨用锰钢的原因是 。
(3)出口处的广告架是金属经焊接而成的,焊条的熔点 (填“>”、“=”或“<”)组成焊条的纯属金属的熔点。
Ⅳ.金属的活动性
康康到工地了解了部分金属材料的防锈问题。技术人员告诉他,采用镀锌钢管做水管时,最好不要用铜质接头。为了探究这三种金属的活动性,康康把等表面积的铁片和锌片放入硫酸铜溶液中(如图所示)。请回答:
(4)如何判断它们是否发生了化学反应?
(5)甲试管中反应前后溶液的质量(填“增重”、“不变”或“减轻”),乙试管中发生反应的化学方程式为 。
(6)上述实验不能够完全证明三种金属的活动性,需要补充的实验操作是 。
Ⅴ.郑州地铁1号线每车次运送乘客约1800人,走同样的路线,CNG公交车每车次消耗天然气akg(以甲烷计算),每辆CNG公交车运送乘客以60名计。若乘CNG公交车的乘客均改乘地铁1号线,则地铁每运行一车次,可减少二氧化碳排放多少千克?