小林、小军和小明在实验室用右图装置做CaCO3受热分解的实验,加热一段时问后,他们对试管内固体的成分进行探究。
【提出问题】加热CaCO3后试管内的固体成分是什么?
【建立假设】小林的假设:CaCO3未分解,固体成分为CaCO3;
小军的假设:CaCO3完全分解,固体成分为 ;
小明的假设:CaCO3部分分解,固体成分为 。
【收集证据】(1)小军取少量固体于试管中,加适量水振荡后静置,再滴
几滴无色酚酞试液,溶液变红。可知小军加水时发生反应的
化学方程 式为————————。
(2)小明向小军实验后的试管中滴加过量稀盐酸,发现有气泡生成。
【获得结论】通过实验可知 的假设是成立的。
【交流与评价】实验结束后,在组内交流讨论过程中部分同学提出:在实验中若增加下列仪器中的 (填编号)就可以直接根据实验现象判断CaCO3是否分解。
工业上用碳酸钠溶液与石灰水反应制烧碱。对于碳酸钠溶液与石灰水是否恰好完全反应,某化学兴趣小组的同学将其产物进行过滤,并对滤液进行如下探究。
【提出问题】滤液中含有哪些溶质?
【猜想与假设】假设一:滤液中只含氢氧化钠假设二:滤液中含氢氧化钠和碳酸钠
假设三:滤液中含
假设四:滤液中含氢氧化钠、氢氧化钙和碳酸钠
【进行实验】甲同学设计了如下实验方案:
| 实验步骤 |
实验现象 |
结论 |
| 取少量滤液放在试管中,再滴入氯化钙溶液 |
若生成白色沉淀 |
碳酸钠过量 |
| 若无明显现象 |
恰好反应 |
【反思与评价】
(1)碳酸钠溶液与石灰水反应的基本类型为 。
(2)乙同学认为假设四不合理,理由是 。
(3)丙同学认为甲同学设计方案还不能说明碳酸钠溶液和澄清石灰水恰好完全反应,她的理由是 。
(4)丁同学认为要说明碳酸钠溶液与石灰水是否恰好完全反应,还需在甲同学实验方案的基础上进行实验。她的实验方案是:
| 实验步骤 |
实验现象和结论 |
【定量研究】
(5)戊同学称取100g烧碱固体样品(样品中的杂质是碳酸钠),加水溶解得到溶液A,取A溶液的1/5向其中加入CaCl2溶液。反应时CaCl2溶液与沉淀的质量关系如图所示。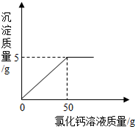
①样品中氢氧化钠的质量为 g;
②计算所加CaCl2溶液中溶质的质量分数。(写出计算过程)
探究蔗糖的元素组成:
提出问题:蔗糖是我们经常接触的一种食品,你是否想过蔗糖是由哪些元素组成的呢?
猜想:生活中,我们偶尔会看见蔗糖在锅里加热时间过长,会变成褐色。因此,你猜想蔗糖中含碳元素,或许还有其他元素。
【收集资料】
(1)蔗糖属于有机化合物(一般指含有碳元素的化合物),所以蔗糖是________(填“纯净物”或“混合物”)。有机化合物一般可以燃烧,受热容易分解,这都属于有机化合物的________性质(填“物理”或“化学”)。
(2)________是化学变化中的最小粒子,因此,在化学反应前后,元素的种类________(填“变多”“不变”或“变少”)。
【设计实验】
(1)将蔗糖在氧气中点燃,分别用干、冷的玻璃片和蘸有澄清石灰水的玻璃片置于火焰上方,观察现象。
①上述实验能证明蔗糖中含有什么元素,如何证明?_________________。
②利用燃烧实验能不能证明蔗糖中含有氧元素,为什么?_________________。
(2)蔗糖隔绝空气加热时发生了分解,得到了黑色的炭,同时容器壁上有小水珠生成。此实验________(填“能”或“不能”)证明蔗糖中含有氧元素。
【实验结论】蔗糖是由______、______、______三种元素组成的(填元素符号)。
实验室里有一瓶常用的无色溶液,因保管不当,其残缺的标签中只剩下“Na”和“10%”字样(如图所示).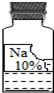
小强和小华同学很感兴趣,决定对其成分进行探究.
【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】根据受损标签的情况判断,这瓶试剂不可能是 ()
A.酸B.碱C.盐
【查阅资料】
Ⅰ初中常见含钠的化合物有:NaCl、NaOH、Na2CO3、NaHCO3.
ⅡNa2CO3和NaHCO3的水溶液都呈碱性.
Ⅲ室温(20℃)时,测定四种物质的溶解度数据如下:
| 物质 |
NaCl |
NaOH |
Na2CO3 |
NaHCO3 |
| 溶解度g |
36 |
109 |
215 |
9.6 |
小华根据试剂瓶标注的质量分数为10%和上表中的溶解度数据判断,这瓶试剂不可能是
【作出猜想】①可能是NaCl;②可能是Na2CO3;③可能是
【实验探究】
(1)小强用洁净的玻璃棒蘸取试液于pH试纸上,测得pH>7,则这瓶试剂不可能是
(2)小强为了检验该溶液是NaOH溶液还是Na2CO3溶液,他又进行了如下实验.
| 实验步骤 |
实验现象 |
结论及化学方程式 |
| 取少量溶液于试管中,滴加 |
产生大量气泡 |
反应的化学方程式: |
| ② 把产生的气体通入澄清的石灰水中. |
澄清的石灰水变浑浊 |
猜想②正确. 反应的化学方程式: |
研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
【假设】H2O2生成O2的快慢与催化剂种类有关
【实验方案】常温下,在两瓶同质量、同浓度的H2O2溶液中,分别加入相同质量的MnO2和水泥块,测量各生成一瓶(相同体积)O2所需的时间。
【进行实验】下图是他们进行实验的装置图,气体发生装置中A仪器名称是____________,此实验中B处宜采用的气体收集方法是______________。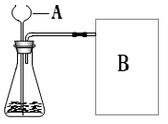
【实验记录】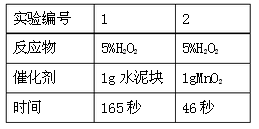
【结论】该探究过程得出的结论是_____________。
【反思】H2O2在常温下分解缓慢,加入MnO2或水泥块后反应明显加快,若要证明MnO2和水泥块是该反应的催化剂,还需要增加实验来验证它们______________。H2O2生成O2的快慢与哪些因素有关?请你帮助他们继续探究。(只要求提出一种影响H2O2生成O2的快慢的因素以及相关假设和实验方案)
【假设】________________
【实验方案】________________
某食品包装袋内有一个小纸袋,上面写着“干燥剂,主要成分是生石灰”。
(1)生石灰可作干燥剂的理由是(用化学方程式表示):______________。
(2)某同学对此干燥剂作了一系列探究,其实验方案如下,请你完成下列实验报告。
| 问题与猜想 |
实验步骤 |
实验现象 |
实验结论 |
| 问题1:小纸袋中的物质能否继续作干燥剂? |
取适量小纸袋中固体放入烧杯中,加入适量水,触摸杯壁。 |
_____________ |
不能作干燥剂 |
| 问题2:猜想变质后的物质可能是什么? ________________。 |
______________ |
_____________ _____________ |
变质后固体中有___________ |