下列装置能构成原电池的是( ) 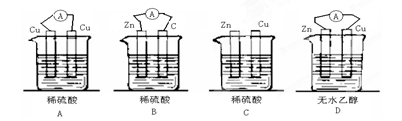
有五组同族元素的物质,在101.3kPa时测定它们的沸点( )如下表所示:
)如下表所示:
对应表中内容,下列各项中正确的是
A.a、b、c的化学式分别为 、 、 、 、 |
| B.第②组物质均有氧化性;第③组物质对应水溶液均是强酸 |
C.第④组中各化合物的稳定性顺序为: |
| D.上表中同族物质对应的氢化物的沸点,均随相对分子质量的增大而升高 |
 电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是
电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是 。电池的总反应可表示为:
。电池的总反应可表示为:
下列说法错误的是
A.该电池工作时,正极反应为: |
B.锂电极作该电池负极,负极反应为: |
| C.该电池工作时,电子通过外电路从正极流向负极 |
| D.该电池组装时,必须在无水无氧条件下进行 |
根据判断,下列各元素一定属于主族元素的是
| A.X元素能形成+7价的含氧酸及其盐 |
| B.Y元素的原予最外电子层上有2个电子 |
| C.短周期元素一定属于主族元素 |
| D.Z元素的阴离子与同一周期稀有气体元素原子的电子层结构相同 |
右图是一个一次性加热杯的示意图。当水袋破裂时,水与固体碎块混和,杯内食物温度逐渐上升。制造此加热杯可选用的固体碎块是
| A.硝酸铵 | B.生石灰 |
| C.氯化镁 | D.石灰石 |
下列有关离子方程式与所述事实相符且正确的是
A.用惰性电极电解 溶液: 溶液: |
B. 溶液中滴加 溶液中滴加 溶液至中性: 溶液至中性: |
C.用氯化铁溶液和沸水反应制取氢氧化铁胶体: |
D.碳酸钙和足量盐酸反应: |