根据碘与氢气反应的热化学方程式:
(i) I2(g)+ H2(g)  2HI(g) △H="-" 9.48 kJ/mol
2HI(g) △H="-" 9.48 kJ/mol
(ii) I2(s)+ H2(g)  2HI(g) △H=+26
2HI(g) △H=+26 .48 kJ/mol
.48 kJ/mol
下列判断正确的是( )
| A.254 g I2(g)中通入2gH2(g),反应放热9.48 kJ |
| B.1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ |
| C.反应(i)的产物比反应(ii)的产物稳定 |
| D.反应(ii)的反应物总能量比反应(i)的反应物总能量低 |
下列叙述不正确的是()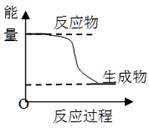
| A.化学平衡发生移动,平衡常数不一定发生变化 |
| B.升高温度会增大化学反应速率,原因是增加了活化分子的百分数 |
| C.某化学反应的能量变化如上图所示,则该反应的△H>0,△S>0 |
| D.H3PO4的电离常数:K1>>K2>>K3 |
铜粉放入稀硫酸溶液中,加热后无明显现象发生。当加入一种盐后,铜粉的质量减少,溶液呈蓝色,同时有气体逸出,该盐是()
| A.Fe2(SO4)3 | B.Na2CO3 | C.KNO3 | D.FeSO4 |
在下列所示的转化关系中,x不可能是()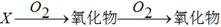
| A.N2 | B.Si | C.Na | D.C |
下列由相关实验现象所推出的结论正确的是( )
| A.Cl2、SO2均能使品红溶液褪色,说明二者均有氧化性 |
| B.向溶液中滴加酸化的Ba(NO3)2溶液出现白色沉淀,说明该溶液中一定有SO42- |
| C.Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应 |
| D.分别充满HCl、NH3的烧瓶倒置于水中后液面均迅速上升,说明二者均易溶于水 |
在一密闭容器中,反应aA(g)  bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则( )
bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则( )
| A.平衡向逆反应方向移动了 | B.物质A的转化率减小了 |
| C.物质B的质量分数增加了 | D.a>b |