某小组为研究电化学原理,设计如图装置。下列叙述正确的是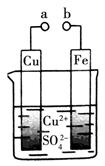
| A.a和b不连接时,铁片上不会有金属铜析出 |
| B.a和b用导线连接时,铁片上发生的反应为:Cu2++2e-→Cu |
| C.无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色 |
| D.a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动 |
在下列给定条件的溶液中,一定能大量共存的离子组是
| A.无色溶液:Ca2+、H+、Cl-、HSO3- |
| B.能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3- |
| C.Na2CO3溶液:K+、Fe3+、SO42-、NO3- |
D.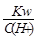 =0.1 mol/L的溶液:Na+、K+、SiO32-、NO3- =0.1 mol/L的溶液:Na+、K+、SiO32-、NO3- |
对于可逆反应mA(g)+nB(g) pC(g)+gD(g),若其它条件都不变,只是在反应前是否加入催化剂,可得到两种υ~t图象如下图
pC(g)+gD(g),若其它条件都不变,只是在反应前是否加入催化剂,可得到两种υ~t图象如下图
如下关系正确的为
①a1=a2 ②a1<a2 ③b1=b2 ④b1<b2 ⑤t1>t2
⑥t1=t2 ⑦两图中阴影部分面积相等 ⑧下图阴影部分面积更大
| A.②④⑤⑦ | B.②④⑥⑧ | C.②③⑤⑦ | D.②③⑥⑤ |
在容积固定的密闭容器中存在如下反应: A(g)+3B(g)  2C(g) △H<0某研究小组研究其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:
2C(g) △H<0某研究小组研究其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:
下列判断正确的是
| A.图I研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高 |
| B.图Ⅱ研究的是压强对反应的影响,且甲的压强较高 |
| C.图Ⅱ研究的是温度对反应的影响,且甲的温度较低 |
| D.图Ⅲ研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较高 |
在可逆反应2SO2+O2 2SO3的平衡状态下,保持恒温恒容向容器中加入一定量的O2,下列说法正确的是(K为平衡常数,QC为浓度商)
2SO3的平衡状态下,保持恒温恒容向容器中加入一定量的O2,下列说法正确的是(K为平衡常数,QC为浓度商)
| A.QC 不变,K变大,O2转化率增大 |
| B.QC 不变,K变大,SO2转化率增大 |
| C.QC 变小,K不变,O2转化率减小 |
| D.QC 增大,K不变,SO2转化率增大 |
有① Na2CO3溶液 ② CH3COONa溶液 ③ NaOH溶液各25mL,物质的量浓度相等,下列说法正确的是
| A.3种溶液pH的大小顺序是 ③>②>① |
| B.若分别滴加25mL和上述溶液等浓度的盐酸后,pH最大的是① |
| C.若将3种溶液稀释相同倍数,pH变化最大的是② |
| D.若3种溶液的pH均为9,则物质的量浓度的大小顺序是③>①>② |