现有T、X、Y、Z短周期元素,其中T元素原子M层上有6个电子,X元素原子最外层电子数是次外层电子数的2倍,Y单质为双原子分子,其氢化物水溶液呈碱性,Z元素最高正价是+7价。
(1)元素Y与氢元素形成一种离子YH4+,写出该微粒的电子式 (用元素符号表 示)
示)
(2)元素Z与元素T相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是 (填序号)。
(用元素符号表示),下列表述中能证明这一事实的是 (填序号)。
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(3)比较等浓度的Na2XO3溶液中c(XO32-)和NaHXO3溶液中c(HXO3-) 大小,
大小,
c(XO32-) c(HXO3-)(填“>” “=”或“<”)
(4)A、J为常见的金属,G为T元素的最高价氧化物对应的水化物,B的溶液呈蓝色。
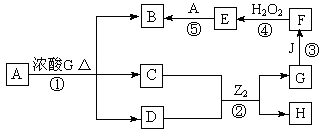
请回答下列问题:
①写出H的化学式____________________;
②写出反应①的化学方程式______________________________;
③写出酸性条件下反应④的离子方程式______________________________。
某微粒的结构示意图为 , 试回答:
, 试回答:
(1)当x-y=10时,该粒子为(选填“原子”或“阳离子”、“阴离子”)。
(2)当y=8时,该粒子可能是(用化学式表示,任填3种)、、。
(3)请写出实验室制取y=7时元素对应单质的离子方程式:。
如图为直流电源电解稀Na2SO4水溶液的装置。通电后在石墨电极a和b附近分别滴加一滴石蕊试液,下列实验现象中正确的是()
| A.逸出气体的体积a电极的小于b电极的 |
| B.一电极逸出无味气体,另一电极逸出刺激性气味气体 |
| C.a电极附近呈红色,b电极附近出现蓝色 |
| D.a电极附近呈蓝色,b电极附近出现红色 |
利用生活中常见的材料可以进行很多科学实验,甚至制作出一些有实际应用价值的装置来,如图就是一个用废旧材料制作的可用于驱动玩具的电池的示意图。当电池工作时,有关说法正确的是()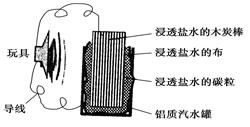
| A.铝罐将逐渐被腐蚀 |
| B.碳粒和炭棒上发生的反应为:O2+4e-=2O2- |
| C.炭棒应与玩具电机的负极相连 |
| D.该电池工作一段时间后炭棒和碳粒的质量会减轻 |
Ⅰ.溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
| 苯 |
溴 |
溴苯 |
|
| 密度/g·cm-3 |
0.88 |
3.10 |
1.50 |
| 沸点/℃ |
80 |
59 |
156 |
| 水中溶解度 |
微溶 |
微溶 |
微溶 |
按以下步骤回答问题:
(1)在a中加入15 mL无水苯和少量铁屑。在b中小心加入4.0 mL 液态溴。向a中滴入几滴溴,a中液体立即沸腾,并有红棕色蒸气出现;a中发生反应的化学方程式为:;继续滴加至液溴滴完。仪器a的名称是;装置d中的作用是。仪器c为冷凝管,其进水口为(填“上”或“下”)口
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10 mL水,然后过滤除去未反应的铁屑;
②滤液依次用10 mL水、8 mL10%的NaOH溶液、10 mL水洗涤。NaOH溶液洗涤的作用是;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是。
(3)经过上述分离操作后,粗溴苯中还含有的主要杂质为,要进一步提纯,下列操作中必须的是。
A.重结晶B.过滤C.蒸馏D.萃取
Ⅱ.用如图所示装置进行实验,将A逐滴加入B中: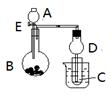
(1)若B为Na2CO3粉末,C为C6H5ONa溶液,实验中观察到小试管内溶液由澄清变浑浊,则试管C中化学反应的离子方程式:。
(2)若B是生石灰,观察到C溶液中先形成沉淀,然后沉淀溶解.当沉淀完全溶解,恰好变澄清时,关闭E然后往小试管中加入少量乙醛溶液,再往烧杯中加入热水,静置片刻,观察到试管壁出现光亮的银镜,则A是(填名称),C是(填化学式),与乙醛的混合后,该溶液中反应的化学方程式:。
某研究小组以甲苯为主要原料,采用以下路线合成医药中间体F和Y。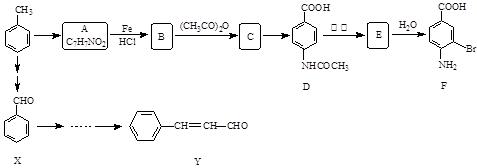
已知: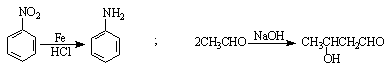
请回答下列问题:
(1)下列有关F的说法正确的是。
| A.分子式是C7H7NO2Br | B.能形成内盐 |
| C.能发生取代反应和缩聚反应 | D.1 mol的 F最多可以和2 mol NaOH反应 |
(2)C→ D的反应类型是 。
(3)B→C的化学方程式是 。在合成F的过程中,B→C步骤不能省略,理由是。
(4)写出同时符合下列条件的A的同分异构体的结构简式。(要求写出3种)
①苯环上只有两种不同化学环境的氢原子;
②分子中含有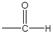 。
。
(5)以X和乙烯为原料可合成Y,请设计合成路线(无机试剂及溶剂任选)。
注:合成路线的书写格式参照如下示例流程图: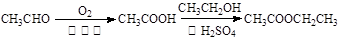
。