(7分)某兴趣小组同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验。请你与他们一起完成以下探究活动:
【对固体猜想】
猜想I:全部是Na2CO3,猜想的依据是 ;
猜想Ⅱ:全部是NaOH 猜想HI~部分是NaOH,部分是Na2CO3。
【实验和推断】
| 实验步骤 |
实验现象 |
| ①取少量白色固体于试管中,加水振荡后,至全部溶解。 |
无色溶液 |
| ②向试管的溶液中滴加适量物质X的溶液 |
现象A |
| ③再向试管中滴加几滴酚酞试液。 |
现象B |
(1)若现象A为有气泡产生,则加入的X溶液是 ,说明氢氧化钠已经变质,有气泡产生的反应的化学方程式是 。
(2)若X是Ca(OH)2溶液,现象A有白色沉淀,现象B为无色酚酞试液变红色,则白色沉淀为 (填化学式),该实验 (填“能”或“不能”)说明样品中有NaOH。
(3)若X是CaCl2溶液,猜想Ⅲ成立的实验现象是 、
。
实验室常用加热氯酸钾与二氧化锰混合物的方法制取氧气,写出反应的化学方程.
小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
【提出猜想】除
、
外,
也可以作
分解的催化剂。
【完成实验】按下表进盈塞坠:羞冽定盆解温度(分解温度越低,催化效果越好)。
| 实验编号 |
实验药品 |
分解温度(
) |
| ① |
580 |
|
| ② |
、
(质量比
) |
350 |
| ③ |
、
(质量比
) |
370 |
| ④ |
、
(质量比
) |
390 |
【分析数据、得出结论】(1)由实验与实验④对比,证明猜想合理
(2)实验所用的三种金属氧化物,催化效果最好的是。
【反思】(1)若要证明
是该反应的催化剂,还要验证它在化学反应前百丽质量和不变;
(2)同种催化剂,颗粒大小可能影响催化效果,请设计实验方案进行验证.
(3)同种催化剂,还有哪些因素可能影响催化效果,请你再探究 (探究一种因素即可)。.
暖宝宝是一种防寒用品,如图所示。暖宝宝中的主要成分有哪些?发热的原因是什么?
(1)小明探究:暖宝宝中的主要成分是什么?
剪开内包装袋,倒出其中的粉末,发现呈黑色。
【提出猜想】该黑色粉末可能含有炭粉、铁粉、二氧化锰、氧化铜、四氧化
三铁中的一种或几种。
【初步验证】将磁铁靠近黑色粉末,部分被吸引。
【查阅资料】四氧化三铁具有磁性,能被磁铁吸引。
【得出结论】该黑色粉末可能含有。
【进行实验】
| 实验编号 |
实验操作 |
实验现象 |
| ① |
取黑色粉末加足量稀硫酸 |
固体部分溶解,有气泡产生,溶液无蓝色 |
② |
取实验①的残渣灼烧,将内壁涂有 澄清石灰水的小烧杯罩在上方 |
澄清石灰水变浑浊 |
由实验①可知,该黑色粉末肯定含,肯定不含.;写出实验①的化学反应方程式。
由实验②可知,该黑色粉末肯定含。(2)小明思考:暖宝宝为什么会发热?
【查阅资料】暖宝宝中的铁粉在空气中发生了缓慢氧化,进而放出热量。
由此可见,人们可以利用化学反应放出的能量,请再举一例:。(3)人们利用化学反应还可以。
某校科技节的实验比赛中,老师先向大家展示了
三瓶白色粉末,然后取一些
固体于研钵中,接着用一纸板挡住同学们的视线,告诉大家打算继续取
在研钵中混合。过一会儿老师拿开纸板,向同学们展示研钵中的白色粉末。
请设计一个实验方案,判断老师是否取了
于上述研钵中。叙述实验操作、预期现象和结论。
提供的试剂有:稀
、蒸馏水、
溶液、
溶液
| 实验操作 |
预期现象与结论 |
| ,说明老师取了
|
|
| ,说明老师取了
|
氢化钙(
)固体是一种储氢材料,是登山运动员常用的能源提供剂。
【阅读资料】
①碱石灰是氧化钙和氢氧化钠的混合物。
②钙遇水立即发生剧烈反应生成氢氧化钙和氢气。
③氢化钙要密封保存,遇水反应生成氢氧化钙和氢气。
【氢化钙的制备】
氢化钙通常用氢气与钙加热制得。某化学兴趣小组设计的制取装置如图10所示(固定装置省略)。
图10
回答下列问题:
(1)装置A中制取氢气的化学方程式为。
(2)装置B的作用是。
(3)装置C中制取氢化钙的化学方程式为。
(4)若不改变温度,整套装置气密性的检查方法是。
【产品的定量测定】
通过上述方法制得的氢化钙样品中常混有未完全反应的钙(其余可能的杂质忽略不计)。样品纯度的测定步骤如下:
①检查装置气密性,装入药品,按图11(固定装置省略)所示连接仪器。
②调整水准管高度,使量气装置两边的液面保持同一水平。读取液面所在的刻度数据为10.0 mL。
③将Y形管慢慢倾斜,直到A端的水全部与B端的样品混合。
④反应结束,冷却至室温,再次读取液面所在刻度数据为110.0 mL。
回答下列问题:
(5)如何判断样品与水完全反应:。
(6)反应生成氢气的体积为mL。
(7)已知该实验条件下,氢气的密度为0.09 mg/mL。样品中氢化钙的纯度为。(结果精确到0.1%)
为判断某物质存在或某物质恰好完全反应,通常以特定物质的显色达到目,能显色的物质就称"指示剂".如:用蓝色的石蕊试纸变红判断待测液显酸性;用淀粉溶液变蓝判断单质碘(
)的存在:
已知:★
(无色溶液);
★常温下,碘微溶入水;
★
(无色溶液).
(1)工业上测量
,
,
混合气体的
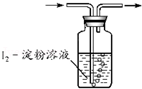
含量用如图吸收装置(量气装置省略).
①混合气体通过图示吸收装置一定时间后,当溶液颜色由蓝色变为色时即可停止通气.此法适宜测
含量较(选填"低"或"高")的混合气体.
②吸收装置内的
的淀粉溶液一也可以用溶液代替作为指示剂.因为.
(2)若用10.0%的氢氧化钠溶液16.0g滴加到20.0g盐酸中(含2滴酚酞试液),混合液刚好由无色变为粉红色时,可认为恰好完全反应.
①原盐酸中溶质的质量分数为.
②试列式计算说明将该反应后的溶液转化为20℃时饱和溶液的一种简单方法(计算结果精确到0.1g).已知:20
时氯化钠的溶解度为36g.