(8分)CO2是初中化学重点研究的气体之一。某化学兴趣小组设计了如下实验来探究CO2的制取和性质:

(1)该兴趣小组用干燥管、烧杯、铜网等设计装配了一个在实验室中制取二氧化碳气体的装置,如右图所示。在干燥管内的铜网上应盛放 ;若将铜网换成铁网,可能产生的后果是 ,其原因是(用化学方程式表示) 。
(2)该兴趣小组同学将制得的CO2分别通人澄清石灰水和氢氧化钠溶液中,他们观察到前者变浑浊,后者无明显现象。CO2和NaOH是否发生了化学反应?
①小明设计了甲、乙两个实验来验证C02与NaOH发生了化学反应,如右图所示。实验现象为:甲——软塑料瓶变瘪,乙——“瓶吞鸡蛋”。
小虎同学认为上述实验是可行的。其共同原理是 。
小雯同学提出质疑,她认为上述实验还不足以说明CO2和NaOH发生了反应。其理由是
。
小明同学针对小雯的质疑又补充了一个对照实验,这个实验是
。
②小虎向甲实验后变瘪塑料瓶的溶液中加入 ,观察到
现象,从而证明CO2与NaOH已经发生了反应。
(3分)请回答下列有关金属的问题。
(1)右边是某探究实验装置图。一段时间后,能观察到什么现象?(装置气密性良好,且开始时U型管两端的红墨水液面相平)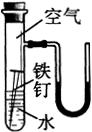
(2)X、Y、Z是三种金属固体,将X和Y浸入稀硫酸中,Y溶解并产生氢气,X无变化;将X和Z浸入硝酸银溶液中,X表面有银析出而Z无变化。
①判断X、Y、Z和银四种金属的活动性由强到弱的顺序。
②具体确定一种X后,写出X与硝酸银溶液反应的化学方程式。
由于大量使用一次性塑料方便袋而造成的“白色污染”已成为一个严重的社会问题。某化学研究小组的同学对某种塑料袋的组成进行分析研究(资料显示该塑料只含C、H两种元素)。他们设计了如图所示的实验装置,使该塑料试样在纯氧中完全燃烧,观察实验现象、分析有关数据、推算元素含量。(碱石灰可吸收水和二氧化碳)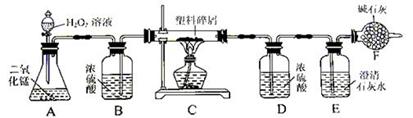
(1)实验装置中有一处明显错误,请写出改正方法.
(2)装置A中反应的化学方程式为.
(3)装置E中的现象是,装置F的作用是
(4)若装置C的玻璃管中放入的塑料试样质量为5.9g,塑料试样充分燃烧后,装置D增重7.2g,则该塑料试样中含氢元素的质量为g;
(5)若装置中没有连接装置B,将使该塑料试样中氢元素的质量测算结果( 填“偏小”、“ 偏大”或“无影响” )
小丽午餐时买了一份清炒菠菜和一份豆腐肉片汤,但同学告诉她菠菜不能与豆腐同食。
[发现问题]菠菜为什么不能与豆腐同食?
[查阅资料]a.制作豆腐需要加入石膏(主要成分:CaSO4);
b.菠菜中含有草酸、草酸盐等成分;
c.草酸钙是一种既不溶于水也不溶于醋酸的白色固体,是诱发人体结石的物质之一。
[提出猜想]菠菜与豆腐同食可能会产生人体不能吸收的沉淀物。
[设计实验]
| 实验步骤 |
实验现象 |
实验结论 |
| ①将菠菜在少量开水中煮沸2~3min,取l~2mL滤液于试管中,并滴加少量_____溶液。 |
产生白色沉淀 |
有草酸钙生成 |
| ②在步骤①的沉淀物中加入过量醋酸 |
沉淀部分溶解,且产生气泡 |
被溶解的沉淀一定不是_____ |
[发现新问题]被溶解的沉淀是什么?产生的气体又是什么?于是她又设计如下实验进一步探究:
| 实验步骤 |
实验现象 |
实验结论 |
| ③将步骤②产生的气体通入中 |
产生的气体是;步骤②被溶解的沉淀是碳酸钙 |
[反思与应用]
(1)家庭中常常将菠菜放在开水中烫过后再烹饪,其目的是
(2)联想到人体胃液中含有盐酸,请提出一个你想要探究的关于食用菠菜的新问题:
氯化钠是日常生活的必需品,也是重要的化工原料。
(1)粗盐除含NaCl外,还含有少量MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是粗盐提纯的操作流程。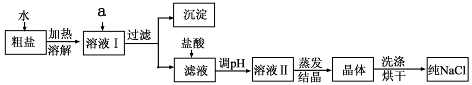
提供的试剂:Na2CO3溶液、K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、饱和NaCl溶液。
①欲除去溶液I中的MgCl2、CaCl2、Na2SO4,从提供的试剂中选出a所代表的试剂,按滴加顺序依次为:过量的NaOH溶液、、;
②在滤液中加盐酸的作用是;
(2)用提纯的NaCl配制200g0.9%的生理盐水,需要NaCl的质量为g。
①配制该溶液时所需要的玻璃仪器有玻璃棒、和,其中玻璃棒在该实验中所起的作用是_____ ___。
②如果配制后溶液溶质的质量分数低于0.9%,你认为可能的原因是。(任写一个)
某同学做“证明鸡蛋壳的主要成分是碳酸盐,并收集纯净的气体”的实验。设计了如下方案进行实验: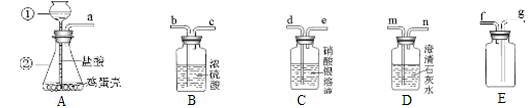
(1)写出所标仪器的名称:①、②。
(2)描述A中发生的现象:。
(3)根据我们所学的知识,你认为A装置和装置相连并产生什么现象时就足以说明鸡蛋壳的主要成分是碳酸盐?。
(4)该同学想要收集一瓶纯净的该气体,再进一步验证它的性质。连接上述装置的顺序是:a→____→____→____→____→____(填写各接口字母)。其中,C装置的作用是_
_,有关反应的化学方程式:。
(5)写出用A装置还可以制取的日常生活中一种常见气体的化学反应方程式:。并说出它的一个重要用途。