(12分)化学实验是学习化学的基础,请根据下列装置图回答问题。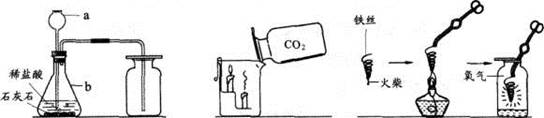
A B C
(1)写出仪器a、b的名称_______;b_______。
(2)写出A图中产生气体的化学方程式____________________________。
(3)B图中,把二氧化碳气体慢慢倒入放有燃着的蜡烛的烧杯中,下层蜡烛先灭,说明二氧化碳具有_______、_______和_______性质。这一性质在实际生活中的应用为_______。
(4)C图中螺旋状铁丝的末端系一根火柴的作用是_______。
(5)小明按C图实验时,集气瓶炸裂了,其可能的原因是_______。
(6)小明对铁丝在氧气中燃烧为什么会火星四射进行探究。下表是他将纯镁条和不同含碳量的铁丝(镁条和铁丝直径均为0.4mm)放入氧气中燃烧时的实验现象的记录。请你分析回答:
| 物质 |
镁条 |
含碳0.05%的铁丝 |
含碳0.2%的铁丝 |
含碳0.6%的铁丝 |
| 燃烧时 的现象 |
剧烈燃烧,发出 耀眼白光,无火星 |
剧烈燃烧 极少火星 |
剧烈燃烧 少量火星 |
(未填) |
在两支试管中各加入2 mL水,然后分别加入1~2小粒碘或高锰酸钾,振荡,观察现象;然后再向两支试管中分别加1 mL汽油,振荡,静置,观察现象。记录如表所示:
| 溶剂 |
溶质 |
现象 |
| 先加水 |
碘 |
底部仍有碘固体,液体呈浅黄色 |
| 先加水 |
高锰酸钾 |
底部无固体,溶液呈深紫色 |
| 再加汽油 |
碘 |
分层,上层呈深紫色,下层近无色,底部无固体 |
| 再加汽油 |
高锰酸钾 |
分层,上层无色,下层呈深紫色,底部无固体 |
请回答:
(1)加入汽油后,投入碘的试管的上层液体名称是_________;投入高锰酸钾的试管的下层液体的名称是_____________________。
(2)从实验现象可以归纳:碘的溶解性为______________,高锰酸钾的溶解性为____________________。
(3)在科学研究中,若将大量水中溶解的少量碘“富集”起来,你认为可以采取的方法是__________________。
铁、铝、铜是常见的三种金属。同学们发现生活中的铝和铜制品表面一般不用防锈,而铁制品一般需要做防锈处理。
【提出问题】这是不是因为铁、铝、铜三种金属中铁的活动性最强呢?
【实验探究】同学们对这三种金属的活动性顺序展开了探究,请你参与探究并填写空格。
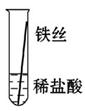
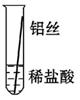
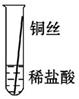
将粗细相同的铁丝、铝丝、铜丝分别插入体积相同、溶质质量分数也相同的稀盐酸中:
| 操作 |
 |
 |
 |
根据现象得出金属活动性顺序 |
| 片刻后现象 |
有少量气泡 |
无气泡 |
无气泡 |
Fe>Al,Fe>Cu |
| 几分钟后现象 |
有少量气泡 |
有大量气泡 |
无气泡 |
【讨论交流】为什么同一个实验得出了两种结论呢?同学们带着这个疑问查阅了相关资料,明白了铝丝在稀盐酸中短时间内无气泡,是因为铝表面致密的氧化膜会先与盐酸反应。
【反思评价】做金属性质实验时需将金属进行打磨,打磨的目的是________。
【实验验证】为了进一步确认铁、铝、铜这三种金属的活动性顺序,同学们又将两根粗细相同的、打磨过的铁丝分别插入硫酸铝溶液、硫酸铜溶液中:
| 操作 |
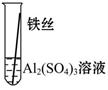 |
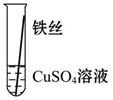 |
根据现象得出金属活动性顺序 |
| 现象 |
无明显现象 |
Al>Fe>Cu |
写出铁与硫酸铜溶液反应的化学方程式_________________。
【拓展迁移】(1)若只有一支盛有少量稀盐酸的试管,只需合理安排金属丝的插入顺序(能与盐酸反应的要一次将盐酸消耗完),也能证明铁、铝、铜这三种金属的活动性顺序。金属丝的插入顺序为________________。
(2)金属被人类大规模开发利用的大致年限也与金属活动性顺序有关,请写出铁、铝、铜三种金属材料被人类利用的先后顺序________________。
下面是对铁的锈蚀条件的探究。因通常实验中铁生锈所需要时间较长,某实验小组设计了如图所示的改进实验。
(1)检查装置的气密性:连接好装置,关闭分液漏斗的旋塞,将C导管接入到装有水的烧杯中,微热甲装置,说明气密性良好的现象是___________________。
(2)反应开始后,甲装置中的反应现象:_______________________,MnO2的作用:__________________。
(3)4分钟后观察:A处铁丝依然光亮,B处铁丝表面灰暗,D处铁丝依然光亮,A、B处实验现象对比,可得出铁生锈与____________有关;B、D处实验现象对比说明:决定铁生锈快慢的一个重要因素是________________________。
某研究性学习小组学习了工业“侯氏制碱法”的原理后,知道如下反应:
NaCl + NH3 + CO2 + H2O = NaHCO3↓+ NH4Cl。
【提出问题】能否在实验室模拟“侯氏制碱法”制取NaHCO3的过程呢?
【实验验证】如下图是该学习小组进行模拟实验时所用到的部分主要装置和药品。
请回答下列问题:
⑴ 检验A装置气密性的方法是:塞紧带长颈漏斗的橡胶塞,夹紧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于试管内的水面,停止加水后,若,说明装置不漏气。
⑵该实验中用B装置制取的气体是(填化学式),B装置中盛装浓氨水的仪器名称为,本实验中使用该仪器的优点是。
⑶D是连接在装置A与装置C之间的气体净化装置,进气口是(填a或b),D的作用是除去HCl气体,反应的化学方程式为。
⑷实验时先向饱和NaCl溶液中通入较多的NH3(溶液显碱性),再通入足量的CO2,其原因是 (填写序号)。
① 使CO2更易被吸收② NH3比CO2更易制取③ CO2的密度比NH3大
⑸用的方法将生成的NaHCO3晶体从混合物中分离出来。
【得出结论】利用“侯氏制碱法”在实验室可以制取NaHCO3 。
同学们在学习了酸碱盐的性质后,萌生了用身边的物质来制取新物质并研究物质性质的想法。请你参与其中,体验实验探究的快乐吧。
【粗产品制备】
课外化学兴趣小组的同学利用家里的纯碱溶液和贝壳为原料制备烧碱,按图所示流程进行实验,请你参与讨论并回答相关问题。
(1)贝壳高温煅烧时,发生反应的化学方程式是 ;
(2)操作Ⅰ是____________,该过程中用到的玻璃仪器有烧杯、 、玻璃棒;
(3)得到烧碱时发生反应的化学方程式为;
(4)得到的溶液存放在如图所示的的瓶中(填A 或B)。
【粗产品成分分析】
将溶液蒸发结晶得到固体C,固体C中的成分有哪些呢?
甲同学认为:只含有NaOH;乙同学认为:只含有NaOH Ca(OH)2;
丙同学认为:含有NaOH Ca(OH) 2Na2CO3;丁认为可能含有。
【分析讨论】:丁同学认为同学的猜想肯定是不合理的,理由是;
(5)甲取少量固体C,加水溶解,向其中滴加3滴酚酞试剂,溶液变为红色,立即得出结论甲的说法正确,你认为甲的结论(填“正确”、“错误”或“无法确定”),理由是 ;
(6)丁取适量固体C溶于水,滴加Ba(NO3)2溶液出现白色浑浊,发生反应的化学方程式为;结论:由上述实验,你认为__________同学的实验结论是正确。
【反思拓展】:在分析化学反应后所得物质的成分时,除了考虑生成物外,还需要虑。
【定量分析】
(7)另称取10g上述样品C,放入盛有100g7.3%的稀盐酸的烧杯中,恰好完全反应,反应后将所得溶液蒸发,求得到的氯化钠固体质量(写出过程2分)。