关于下列装置说法正确的是( )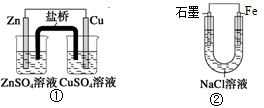
| A.装置①中,盐桥中的K+移向CuSO4溶液 |
| B.装置①中,Zn为负极,发生还原反应 |
| C.装置②中的Fe发生析氢腐蚀 |
| D.装置②中电子由Fe流向石墨,然后再经溶液流向Fe |
在体积都为1L、pH都等于2的盐酸和醋酸溶液中,投入0.65g锌粒,则下列各图所示内容比较符合客观事实的是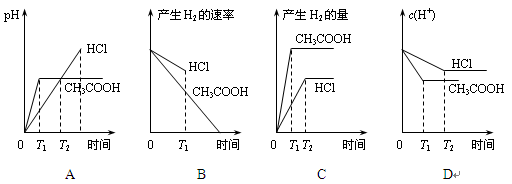
对于可逆反应A(g)+ 2B(g)  2C(g)ΔH>0,下列图象中正确的是
2C(g)ΔH>0,下列图象中正确的是
某温度下,在一固定体积的密闭容器中,进行如下化学反应:H2(g)+I2(g)  2HI(g),下列情况能说明该反应一定达到平衡状态的是
2HI(g),下列情况能说明该反应一定达到平衡状态的是
| A.混合气体的颜色不再改变 |
| B.混合气体的压强不再改变 |
| C.单位时间内拆开1mol H-H键,同时生成2mol H-I键 |
| D.混合气体的密度不再改变 |
下列各组离子,在指定环境中一定能大量共存的是
| A.在含有0.1 mol/L Ca2+的溶液中:Na+、K+、ClO-、Cl- |
| B.在pH为7的溶液中:Ag+、Fe3+、SO42-、Cl- |
| C.在澄清透明的无色溶液中:Al3+、Cu2+、HCO3- 、NO3- |
| D.c(OH-)=1×10-3mol/L的溶液中:K+、SO42-、Cl-、HCO3- |
下列说法正确的是
| A.pH<7的溶液一定显酸性 |
| B.25℃时,pH=5的溶液与pH=3的溶液相比,前者c(OH-)是后者的100倍 |
| C.室温下,每1×107个水分子中只有一个水分子发生电离 |
| D.在0.1mol/L的氨水中,改变外界条件使c(NH4+)增大,则溶液的pH一定增大 |