在氧气性质和制取的试验中,需完成碳和铁丝在氧气中燃烧两实验,实验册提示取用高锰酸钾的质量为7克。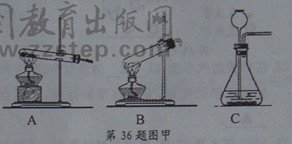
(1)计算分析:小明实验时采用容积为125毫升的集气瓶,如果按实验册提示,他能否制得两瓶氧气?(氧气密度为1.43g/升)
(2)实验操作:
①利用高锰酸钾制取氧气,他应选用如图甲中的发生装置 ;
②制氧时,小明未能收集到两瓶氧气,其可能的原因有 ;
| A.没有塞紧试管塞 |
| B.试管口没有放棉花 |
| C.没有及时更换收集第二瓶 |
| D.加热前已将集气瓶灌满水倒立于水槽中 |
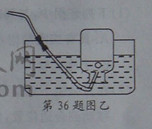
③小明采用图乙方法收集,从水槽中取出充满氧气的集气瓶,正方于实验桌上,发现瓶口上方的玻璃片容易滑动,其原因是 。
称取NaCl和BaCl2的固体混合物32.5g,加入100g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如下图所示。试回答下列问题: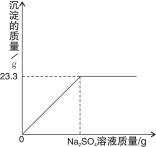
(1)完全反应后生成BaSO4沉淀g。
(2)恰好完全反应时消耗Na2SO4溶液的质量是g。
(3)恰好完全反应时所得溶液中溶质的质量分数是多少?(精确到0.1%)
实验室有一瓶久置的氢氧化钠固体,某同学想了解其变质情况,设计了实验,实验过程如下:
实验一:取少量样品于试管中,滴加适量稀盐酸,观察到有气泡产生,说明氢氧化钠已变质,变质的原因是___________________________(用化学方程式表示)。
实验二: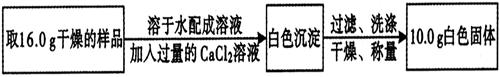
通过实验二,能进一步推算出氢氧化钠变质的程度。请计算实验二中参加反应的碳酸钠质量。
结论:16.0 g干燥的样品中已变质的氢氧化钠的质量是g。
某纯碱样品中含有少量的氯化钠杂质。现称取6g该纯碱样品放在烧杯中并滴加稀盐酸。当盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(假设产生的气体全部逸出),产生气体的质量与滴入稀盐酸的质量关系如下图所示。试回答:
(1)A点产生气体的质量m = 。
(2)B点时,烧杯内溶液中的溶质是(写出化学式)。
(3)A点时溶液中溶质的质量分数(写出计算过程,结果精确到0.1%)。
(1)维生素A的化学式为C20H30O,能维持人体正常的视觉反应。回答下列问题:①一个维生素A分子共含有个原子。
②维生素A 中C、H、O元素的质量比为。
(2)在科学家眼里,二氧化碳是可以利用的重要资源。在一定条件下,二氧化碳和金属钠反应可以制金刚石〖CO2+4Na一定条件C(金刚石)+2Na2O〗。请计算92g金属钠理论上可制得含碳96%的金刚石的质量是多少g?(最后结果保留一位小数)
(4分)将24g由木炭和氧化铜组成的混合物充分加热,其中木炭完全反应,反应结束后将剩余物冷却,称得固体质量为19.6g,请计算:
(1)生成二氧化碳多少克?
(2)反应前混合物中氧化铜的质量分数为多少?