某校化学实验课上,同学们用化学方法探究一种钢样品中铁的含量。同学们将11.4 g钢样品和20.0 g稀盐酸(足量)放入质量为120.0 g烧杯中。在化学反应过程中对烧杯及其中的剩余物进行了四次称量,记录如下表:
| 反应时间 |
T0 |
T1 |
T2 |
T3 |
| 烧杯和药品质量/ g |
151.4 |
151.3 |
151.0 |
151.0 |
(最后结果保留一位小数)
(1)反应中产生氢气的质量是 g。
(2)钢的类型分为:
| 低碳钢 |
中碳钢 |
高碳钢 |
| 含碳量0.03%~0.3% |
含碳量0.3%~0.6% |
含碳量0.6%~2% |
假设残留在烧杯中的黑色固体全部是碳单质,试通过计算判断这种钢属于哪种类型的钢?
(3)某钢厂欲冶炼1000 t这种钢材,需含氧化铁80%的赤铁矿多少吨?
牛奶中的主要营养物质是蛋白质。通常情况下,牛奶中氮元素的含量越高,说明蛋白质的含量也越高,所以可以通过测定氮元素的含量来确定牛奶的质量等级。2008年发生的“三鹿奶粉”事件,举国震惊。该奶粉中被添加一种叫三聚氰胺(C3N6H6)的化工原料,导致食用该奶粉的许多婴幼儿患病,甚至死亡。
(1)三聚氰胺中碳、氮、氢三种元素的原子个数比为________________。
(2)三聚氰胺中氮元素的质量分数是________________,根据三聚氰胺中氮元素的质量分数,请你分析利欲熏心者加三聚氰胺的目的是
在某公共场所张贴有以下广告:
| 化肥广告 -----国际首创----- 优质化肥:碳酸氢铵( 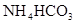 ) )含氮量全球最高:(24.1%) |
请回答下列问题:
(1)该化肥中的碳酸氢铵的相对分子质量为(不要求计算过程,下同)__________________;
(2)该化肥碳酸氢铵中各元素的质量比为氮元素:氢元素:碳元素:氧元素=_________∶_________∶_________∶_________;该化肥中碳酸氢铵中氮元素的质量分数为________,因此这是一则_________(填“真实”或“虚假”)广告(计算结果精确到0.1%)
某同学为了检验家里购买的硫酸铵化肥是否合格,他称取27.5 g化肥样品与足量浓烧碱溶液加热,产生的氨气用100.0g废硫酸吸收。测得吸收氨气的溶液总质量m与反应时间t的变化如右下图所示。所涉及的反应为:
(NH4)2SO4+2NaOH△Na2SO4+2H2O+2NH3↑; 2NH3+H2SO4 ==(NH4)2SO4。
请计算: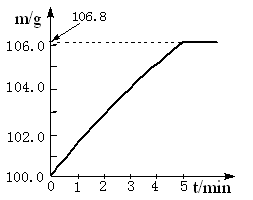
(1)完全反应后产生氨气g。
(2)该化肥的含氮量为 (精确到0.1%),
则这种化肥属于(填:“合格”或“不合格”。
合格硫酸铵含氮量为20%以上)产品。
(3)请计算废硫酸中硫酸的质量分数(写出计算
过程)。
(4)若实验过程中氨气被完全吸收,但该实验测得硫酸铵化肥的含氮量高于实际值,其原因是。
过氧化氢不稳定会自然分解,久置的过氧化氢溶液,其溶质的质量分数会变小。某兴趣小组为测定实验室中一瓶久置的过氧化氢溶液中溶质的质量分数,进行实验。测得相关数据如图9所示: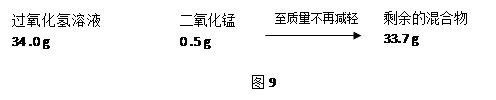
(1)根据质量守恒定律,反应生成氧气的质量为。
(2)计算该过氧化氢溶液中溶质的质量分数。(写出计算过程)
友情提示:实验中过氧化氢分解的化学方程式为 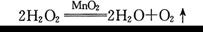
、实验室现有氯化镁和硫酸钠的固体混合物样品,小明同学想测定样品中氯化镁的质量分数。先称取该混合物样品20g,完全溶于水中,然后取用了一定溶质质量分数的氢氧化钠溶液100g平均分四次加入其中,充分振荡,实验所得数据见下表,请你分析并进行有关计算:
 |
1 |
2 |
3 |
4 |
| 加入氢氧化钠溶液的质量/g |
25 |
25 |
25 |
25 |
| 生成沉淀的质量/g |
2.9 |
X |
8.7 |
8.7 |
(1)上表中X的数值为_________;
(2)计算原固体混合物样品中氯化镁的质量分数是多少?
(3)上述实验中所用到的氢氧化钠溶液,是小明同学利用实验室中已有的80g溶质质量分数为30%的氢氧化钠溶液现配制的,试计算需加入多少克水,才能配成实验中所需溶质质量分数的氢氧化钠溶液?