已知苯酚钠溶液中通入二氧化碳,充分反应后只能生成苯酚和碳酸氢钠;而偏铝酸钠溶液中通入二氧化碳时,可生成氢氧化铝和碳酸钠,则下列说法正确的是
| A.酸性:苯酚<氢氧化铝<碳酸 |
B.结合质子的能力:  <HCO3-<CO32-<AlO2- <HCO3-<CO32-<AlO2- |
| C.同温、同浓度下溶液碱性强弱:偏铝酸钠>碳酸钠>苯酚钠>碳酸氢钠 |
| D.相同pH的下列溶液其物质的量浓度:碳酸氢钠>碳酸钠>苯酚钠 >偏铝酸钠 |
下列叙述中不正确的是
| A.将NaAlO2溶液在蒸发皿中蒸干,最终得到的固体物质是Al(OH)3 |
| B.溶液中c(H+)>c(OH—),该溶液一定显酸性 |
| C.用原电池作电源进行电解时,电子从原电池负极流向电解池阴极 |
| D.外加电流的阴极保护法,构成了电解池;牺牲阳极的阴极保护法构成了原电池 |
下列推论正确的是
| A.H2(g)的燃烧热是285.8 kJ·mol-1,则2H2O(g)=2H2(g)+O2(g) ΔH=+285.8 kJ·mol-1 |
| B.对于反应2H2O2==2H2O+O2↑,升高温度能加快O2的生成速率 |
| C.已知2C(s)+2O2(g)=2CO2(g) ΔH1;2C(s)+O2(g)=2CO(g) ΔH2,则ΔH1>ΔH2 |
D.在CuCl2水溶液中存在如下平衡:[Cu(H2O)4]2+(蓝)+4Cl—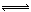 [CuCl4]2—(绿)+4H2O,若向溶液中滴加足量AgNO3溶液,可使溶液呈现绿色 [CuCl4]2—(绿)+4H2O,若向溶液中滴加足量AgNO3溶液,可使溶液呈现绿色 |
25℃时,浓度均为0.1 mol·L-1的HA溶液和BOH溶液,pH分别是1和11。下列说法正确的是
| A.在0.1 mol·L-1BA溶液中,c(A-)+c(H+)=c(BOH)+c(B+) |
| B.若将0.1 mol·L-1 BOH溶液稀释至0.001 mol·L-1则溶液的pH=9 |
| C.若将一定量的上述两溶液混合后pH=7,则混合液中:c(A-)>c(B+) |
| D.若将上述两溶液按体积比1∶1混合,则混合液中:c(A-)>c(B+)>c(H+)>c(OH-) |
某温度下,在一定体积的密闭容器中X、Y、Z、W四种气体的初始浓度和平衡浓度
如下表,下列说法错误的是
| 物质 |
X |
Y |
Z |
W |
| 初始浓度/mol·L-1 |
0.5 |
0.6 |
0 |
0 |
| 平衡浓度/mol·L-1 |
0.1 |
0.1 |
0.4 |
0.6 |
A.增大压强反应的平衡常数不变,但X的转化率增大
B.该反应的化学方程式为:4X (g)+5Y (g) 4Z (g)+ 6W (g)
4Z (g)+ 6W (g)
C.反应达到平衡时,X的转化率为80%
D.其它条件不变,若增大Y的起始浓度,X的转化率增大
对于可逆反应:mA(g)+nB(g) xC(g)+ yD(s) ΔH=?,在不同温度及压强(P1,P2)条件下,反应物A的转化率如下图所示,下列判断正确的是
xC(g)+ yD(s) ΔH=?,在不同温度及压强(P1,P2)条件下,反应物A的转化率如下图所示,下列判断正确的是
| A.ΔH>0,m+n>x+y | B.ΔH<0,m+n>x+y |
| C.ΔH<0,m+n>x | D.ΔH>0,m+n<x |