下述实验设计能够达到目的的是( )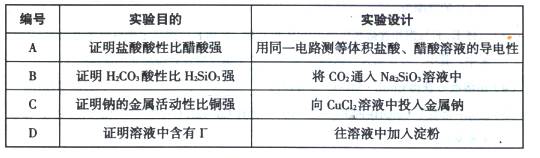
已知温度T时水的离子积常数为KW。该温度下,将浓度为a mol/L的一元酸HA与b mol/L的一元碱BOH等体积混合,可判定该溶液呈中性的依据是
| A.a = b |
| B.混合溶液的pH = 7 |
C.混合溶液中,c(H+) =  mol/L mol/L |
| D.混合溶液中,c(H+) +c(B-) = c(OH-) + c(A-) |
常温条件下,有关① pH=2的CH3COOH溶液;②pH=2的HCl溶液;③pH=12的氨水;④pH=12的NaOH溶液,四种溶液的比较中,正确的是
| A.水电离的c(H+):①=②<③=④ |
| B.将②、③溶液混合后pH=7,则消耗溶液的体积:②=③ |
| C.等体积的①、②、④溶液分别与足量铝粉反应,生成H2的量:④最大 |
| D.向溶液中加入100mL水后,溶液的pH:③>④>②>① |
在300mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni (s)+4CO (g)  Ni(CO)4 (g),已知该反应平衡常数与温度的关系如表:
Ni(CO)4 (g),已知该反应平衡常数与温度的关系如表:
| 温度/℃ |
25 |
80 |
230 |
| 平衡常数 |
5×104 |
2 |
1.9×10﹣5 |
下列说法不正确的是
A. 上述生成Ni(CO)4 (g)的反应为放热反应
B. 25℃时反应Ni(CO)4 (g)  Ni (s)+4CO (g)的平衡常数为2×10﹣5
Ni (s)+4CO (g)的平衡常数为2×10﹣5
C. 80℃达到平衡时,测得n(CO)=0.3mol,则Ni(CO)4的平衡浓度为2 mol/L
D. 在80℃时,测得某时刻,Ni(CO)4、CO浓度均为0.5 mol/L,则此时v(正)>v(逆)
SF6是一种优良的绝缘气体,分子结构中只存在S-F键。已知:1molS(s)转化为气态硫原子吸收能量280kJ,断裂1molF-F 、S-F键需吸收的能量分别为160kJ、330kJ。则S(s)+3F2(g)=SF6(g)的反应热ΔH为
| A.−1780kJ/mol | B.−1220 kJ/mol |
| C.−450 kJ/mol | D.+430 kJ/mol |
下列说法正确的是
| A.等质量的白磷蒸气和白磷固体分别完全燃烧,后者放出的热量多 |
| B.人类日常利用的煤、天然气、石油等的能量,归根到底是由太阳能转变来的 |
| C.燃烧热是指1mol物质完全燃烧时放出的热量 |
| D.H+ (aq)+OH-(aq)=H2O(1) △H=-57.3kJ/mol 也能表示稀醋酸与稀NaOH溶液反应的中和热 |