微型钮扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH,电极反应为:Zn+2OH--2e-==ZnO+H2O;Ag2O+H2O+2e-==2Ag+2OH- 根据上述反应式,判断下列叙述中正确的是( )
| A.在使用过程中,电池负极区溶液的pH减小 |
| B.使用过程中,电子由Ag2O极经外电路流向Zn极 |
| C.Zn是负极,Ag2O是正极 |
| D.Zn电极发生还原反应,Ag2O电极发生氧化反应 |
在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度。则下列说法正确的是
| A.甲的物质的量比乙的物质的量少 |
| B.甲的分子数比乙的分子数多 |
| C.甲的体积比乙的体积大 |
| D.甲的相对分子质量比乙相对分子质量小 |
已知KMnO4与浓HCl在常温下反应就能产生Cl2。 若用右图所示装置来制备纯净、干燥的氯气,并试验它与金属的反应。每个虚线框表示一个单元装置,其中错误的是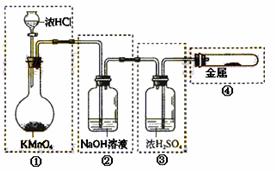
| A.只有①和②处 |
| B.只有②处 |
| C.只有②和③处 |
| D.只有②、③、④处 |
要除去NaCl溶液中含有的Ca2+、Mg2+、SO42-、HCO3-等离子,通常采用以下四种试剂:①Na2CO3②BaCl2③NaOH④HCl。加入试剂合理的操作顺序是
| A.①②③④ | B.③①②④ | C.④②①③ | D.③②①④ |
检验氯化氢气体中是否混有氯气,可采用的方法是
| A.用干燥的蓝色石蕊试纸 | B.用干燥有色布条 |
| C.将气体通入硝酸银溶液 | D.用湿润的淀粉碘化钾试纸 |
3.6gH2与足量的氧气充分燃烧后,立即将全部燃烧产物通过足量的Na2O2固体,最终固体质量将增加
| A.2.1g | B.3.6g | C.7.2g | D.8.4g |