已知浓硝酸是一种易挥发的强酸,见光易分解,其分解的反应方程式为:4HNO3△2H2O+4NO2↑+X↑。根据上述信息,回答下列问题:
⑴浓硝酸的化学性质: (写出一种即可);
⑵水中氢、氧元素的质量比: (最简整数比);
⑶判断X的化学式: ;
⑷二氧化氮分子由氮原子和氧原子构成,其中,氮原子的原子结构示意图为 ,氮原子的最外层上的电子数为: 。
,氮原子的最外层上的电子数为: 。
化学可以从微观角度认识世界,请用微粒的观点回答问题。
(1)氧气和液氧都是由 构成的
(2)氧气可压缩为液氧储存于钢瓶中,说明 。
(3)空气中的氧气无处不在,是 的结果。
(4)氧气与碳发生化学反应时,没有改变的两种粒子是 。
已知甲、乙、丙是初中化学常见的物质,且三种物质中均含有相同的元素。它们的转化关系如图所示(“→”表示一种物质能转化成另一种物质,部分反应物、生成物及反应条件已略去)。
(1)若甲、乙组成元素相同,且乙是最常见的溶剂,则丙是 (填化学式);若乙、丙组成元素相同,且丙是有毒气体,则乙转化成丙是 (填“吸热”或“放热”)反应。
(2)若三种物质都含有铜元素,且分别是单质、氧化物、盐中的一种,则乙、丙相互转化的基本反应类型是 。
(3)若乙是建筑材料大理石的主要成分,且甲是纯碱,则丙转化成乙的化学方程式为 。
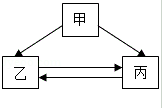
图1是铝元素在元素周期表中的相关信息,图2是几种微粒的结构示意图。
回答下列问题:

(1)铝的相对原子质量为 。
(2)图2中,B所对应的元素位于元素周期表的第 周期。
(3)铝元素和镁元素的本质区别是 。
(4)图2中,属于相对稳定结构的原子是 (填字母序号)。
a、b、c三种固体物质的溶解度曲线如图所示,回答下列问题:
(1)M点的含义是 。
(2)在t2℃时,向盛有50ga物质的烧杯中加入80g水,充分溶解后,所得溶液的质量为 g。
(3)在t1℃时,将a、b、c三种物质的饱和溶液分别升温至t2℃,所得三种溶液溶质的质量分数由大到小的顺序是 。

金属材料在生活中随处可见回答下列问题:
(1)钢和生铁都属于金属材料,它们都是 的合金。
(2)钢铁很容易生锈,用盐酸除铁锈的化学方程式为 。
(3)向一定量的硝酸银和硝酸铜的混合溶液中加入一定量的铁粉,充分反应后过滤,得滤渣和滤液。向滤渣中加入稀盐酸有气泡产生。则滤液中包含的基本粒子是 (用符号表示)。