用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法。其中阴、阳离子交换膜组合循环再生机理如下图所示,则下列有关说法中不正确的是 ( )
| A.X为直流电源的负极,Y为直流电源的正极 |
| B.图中的b>a |
| C.阳极区pH增大 |
| D.该过程中的产品主要为H2SO4和H2 |
某学生想利用下图装置(烧瓶位置不能移动)收集下列气体: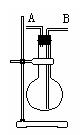
① H2②Cl2③CH4④HCl ⑤NH3⑥NO ⑦NO2⑧SO2,
下列操作正确的是
| A.烧瓶是干燥的,由A进气收集①③⑤ |
| B.烧瓶是干燥的,由B进气收集②④⑥⑦⑧ |
| C.在烧瓶中充满水,由A进气收集①③⑤⑦ |
| D.在烧瓶中充满水,由B进气收集⑥ |
已知下列反应的热化学方程式为:
⑴C(s)+O2(g)=CO2(g)ΔH 1=-393.5kJ/mol
⑵CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH 2=-870.3kJ/mol
⑶H2(g)+1/2 O2(g)=H2O(l) ΔH 3=-285. 8kJ/mol
则反应2C(s)+2H2(g)+O2(g)=CH3COOH(l) 的焓变(ΔH)为
| A.+ 488.3 kJ/mol | B.-488.3 kJ/mol |
| C.-244.15 kJ/mol | D.+ 244.15 kJ/mol |
赤铜矿的成份是Cu2O,辉铜矿的成份是Cu2S,将赤铜矿与辉铜矿混合加热有以下反
应:2Cu2O+Cu2S = 6Cu+SO2↑,对于该反应,下列说法正确的是
| A.该反应的氧化剂只有Cu2O | B.Cu既是氧化产物,又是还原产物 |
| C.每生成1 mol Cu,还原剂转移给氧化剂的电子为2 mol | |
| D.该反应中氧化产物与还原产物的质量比为1∶6 |
用NA表示阿伏加德罗常数的值。下列叙述正确的是
| A.1 L 1 mol·L-1的FeCl3溶液中含有NA个Fe3+ |
| B.标准状况下,22.4 L己烷中共价键数目为19NA |
| C.由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA |
| D.常温常压下的33.6 L氯气与27 g铝反应,转移电子数为3NA |
接触法生产H2SO4的过程中,对废气、废液、废渣和“废热”的处理正确的是
①尾气用氨水处理②污水用石灰乳处理
③废渣用来炼铁、制水泥等④将“废热”通过“废热”锅炉产生蒸气发电
| A.只有①② | B.只有①③④ | C.只有①②③ | D.全部 |