以环戊二烯( )是一种化学活性很高的烃,存在于煤焦油中。
)是一种化学活性很高的烃,存在于煤焦油中。
(1)写出双环戊二烯的分子式 ;
(2)双环戊二烯的各种同分异构体当中,可能含有的官能团有 ;
A.碳碳双键 B.碳碳叁键 C.苯环
(3)室温下发生下列反应: 反应类型为 ;
反应类型为 ;
(4)篮烷( )是双环戊二烯的同分异构体,假设篮烷分子结构示意图中夹角只有135°、90°两种,它的一氯代物有 种。
)是双环戊二烯的同分异构体,假设篮烷分子结构示意图中夹角只有135°、90°两种,它的一氯代物有 种。
铁是自然界里分布最广的金属元素之一,在地壳中的质量约占5%左右。铁矿石的种类很多,重要的有磁铁矿石(主要成分是Fe3O4)、赤铁矿石(主要成分是Fe2O3)等。
(1)写出用赤铁矿石炼铁的主要化学反应方程式。
(2)红热的铁能跟水蒸气起反应,有一种产物是可燃性气体,则其反应的化学方程式为。在常温下,铁跟水不反应,但是,在水和空气里的氧气及二氧化碳等的共同作用下,铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁产量的四分之一。刷油漆是重要的防腐蚀措施之一,油漆防腐蚀的主要原理是。
(3)铁元素是人体的重要营养元素,举一例说明铁元素在人体中的重要作用。
已知有关物质的熔沸点数据如下表:
| MgO |
Al2O3 |
MgCl2 |
AlCl3 |
|
| 熔点/℃ |
2852 |
2072 |
714 |
190 |
| 沸点/℃ |
3600 |
2980 |
1412 |
182.7 |
请参考上述数据填空和回答问题。
(1)工业上常用电解熔融MgCl2的方法生产金属镁,而不用电解电解MgO的方法生产镁。
(2)工业上用电解Al2O3与冰晶石熔融混合物的方法生产铝,而不用电解AlCl3的方法生产铝,冰晶石在炼铝过程中的作用是。
(1)炼钢和炼铁都利用氧化还原反应,但炼铁是有,其核心反应是。而炼钢主要是用,其除碳的反应为。
(2)炼铁时常用的焦炭形成还原剂,能用煤代替吗?,为什么?
(3)检查钢质设备完好性的方法之一是:在被怀疑有裂纹处涂上10%的盐酸,过一段时间如观察到有粗线裂纹,表明该部分原先确有裂纹,产生粗线裂纹的原因是
某种ABS工程树脂,由丙烯腈(CH2= CHCN,符号A)、1,3-丁二烯(符号B,CH2="CHCH=" CH2)和苯乙烯(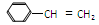 ,符号S),按一定配比共聚而得。
,符号S),按一定配比共聚而得。
(1)A、B和S 三种单体中,碳氢比(C﹕H)值最小的单体是。
(2)经元素分析知该ABS样品的组成为CaHbNc(a、b、c为正整数),则原料中A和B的物质的量之比是(用a、b、c)。
科学家把药物连接在高分子载体上制成缓释长效药剂。阿斯匹林结构为: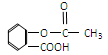 ;它可以连接在一高聚物载体上,形成缓释长效药剂,其中一种的结构简式为:
;它可以连接在一高聚物载体上,形成缓释长效药剂,其中一种的结构简式为: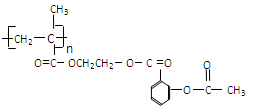
试回答:
(1)缓释长效阿司匹林的载体的结构简式为。
(2)服药后在人体内通过水解作用,可以缓慢地释放出阿司匹林,写出这个水解的化学方程式:。
(3)这种高分子载体是由单体发生聚合反应得到的。写出单体的结构简式。