某化学小组围绕燃烧与灭火的主题开展了相关实验探究活动。请根据实验图示回答问题: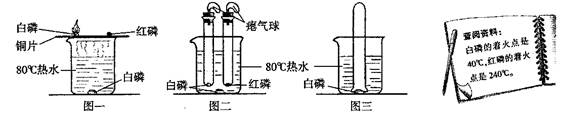
(1)图一实验中可观察到的现象是 ,改进后的装置(如图二)与图一相比,其优点是 。
(2)将装有某气体的大试管口朝下垂直插入水中,使试管罩住白磷(如图三所示),结果观察到了“水火相容”的奇观,则大试管所装气体可能是 ,化学反应方程式为
。
(3)上述实验中可的出,可燃物燃烧的必备条件是 , 。
实验室开放日,某化学兴趣小组的同学在老师的指导下,设计了如下实验装置进行气体制取和性质的探究,请回答有关问题: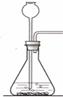
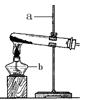
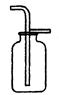



A B C D E F
在化学实验室里,酒精是最常用到的一种燃料,其化学式是C2H6O。小明为了证明酒精中含有碳、氢元素,设计并完成如下实验方案。请你帮他完成下面的实验报告。
【实验目的】:证明酒精中含有碳、氢元素。
【实验用品】:酒精灯、火柴、洁净干燥的小烧杯、澄清石灰水
【实验过程及结论】
| 实验步骤 |
实验现象 |
实验结论 |
| 步骤一:点燃酒精灯,将洁净干燥的小烧杯罩在火焰上方 |
烧杯内壁 有生成; |
证明酒精中含有元素 |
| 步骤二:迅速取下烧杯,并加入少量,振荡; |
证明酒精中含有碳元素 |
我们已经学过实验室制取气体的一般思路和方法,请利用下列装置回答相关问题.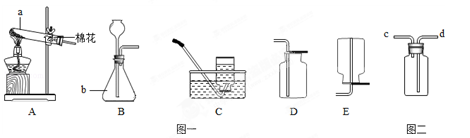
(1)写出图一中a和b的仪器名称:ab;
(2)选择图一中的装置制取和收集二氧化碳气体,那么应选择的装置是和;
在实验室中制取二氧化碳气体的常用药品:液体是,固体是。
(3)若要用图二装置收集二氧化碳气体,则气体应从(填c或d)端通.理由是.
(4)用制取的二氧化碳进行如下有关性质实验:
①实验(II)中溶液变色;
②实验(III)中加热之后,溶液又变为色,解释出现此现象的原因。
(5)实验室用高锰酸钾制取氧气的化学反应方程式(或化学式表达式)若要用排水法收集一瓶较纯净的氧气,开始收集氧气的最佳时机是。
(6)同学称取一定质量的KMnO4固体放入大试管中,将温度控制在250℃加热制取O2。实验结束时,乙同学发现用排水法收集到的O2大于理论产量。针对这一现象,同学们进行了如下探究:
[提出猜想]猜想I:反应生成的MnO2分解放出O2;
猜想II:反应生成的K2MnO4分解放出O2;
猜想III:反应生成的K2MnO4和MnO2分解都放出O2。
[实验验证]同学们分成两组,分别进行下列实验:
第一组同学取一定质量的MnO2,在250℃条件下加热一段时间,冷却后测得MnO2的质量不变,则猜想错误;第二组同学取K2MnO4在250℃条件下加热,没有用测定质量的方法得出了猜想II正确的结论。该组同学选择的实验方法是。
[拓展延伸]实验发现,KClO3固体加热制取O2的反应速率很慢,但如果将KMnO4固体与KClO3固体混合加热,则KClO3的分解速率大大加快。
请说明KMnO4在KClO3的分解反应中是否作催化剂,为什么?。
有一次晚自修时,学校突然停电,同学们点起了蜡烛,不一会儿来电了,大家把蜡烛吹灭,这时看到有一缕白烟,有几个同学对这缕白烟产生了兴趣。
【提出问题】小明想,吹灭蜡烛时观察到的一缕白烟的成分是什么?
【猜想与假设】小亮猜测白烟是蜡烛燃烧产生的二氧化碳;小光猜想白烟是石蜡燃烧产生的水蒸气;小明猜想白烟是石蜡蒸气凝结成的固体颗粒。
【收集证据】
(1)查阅资料:烟是由固体颗粒形成的,雾是由小液滴形成的。石蜡的熔点和沸点都很低,很容易液化和气化。二氧化碳是无色的且能使澄清石灰水变浑浊的气体。
(2)实验探究:①吹灭蜡烛,立即用一个内壁涂有澄清石灰水的烧杯罩住白烟,观察到澄清石灰水。小亮得出结论:白烟是二氧化碳。但小明对此提出质疑,小明认为小亮不正确的原因是。
②吹灭蜡烛,立即用一块干而冷的玻璃片罩在白烟上,玻璃片上没有水雾。小光得出结论:白烟不是。
③吹灭蜡烛,立即用燃着的木条靠近白烟,发现蜡烛重新被点燃,说明白烟具有可燃性,该实验同时排除了的猜想。
【得出结论】以上探究结果可知:的猜想是正确的。
某校化学兴趣小组的同学利用下列装置进行实验。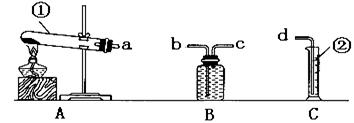
实验目的:
一.用高锰酸钾制取一瓶氧气,做细铁丝燃烧的实验。
二.粗略测定加热2g高锰酸钾所收集到的氧气体积。
反应原理:(用化学式表达式表示)
高锰酸钾制氧气:。
细铁丝在氧气中燃烧: 。
装置连接:
写出标数字的仪器名称:①,②。
为达到实验二的目的,各装置的正确连接顺序是:(填接口的字母)a→→ →d。
问题分析:
(1)实验过程发现B瓶中的水变红了,原因是:。
(2)用收集到的氧气做细铁丝燃烧的实验时,发现瓶底炸裂,发生失误的操作可能是:。
(3)在本实验中,收集氧气的时机是加热后马上收集,若是在气体连续不断产生之后才开始收集,则测得的氧气的体积会比实际值(填“偏大”或“偏小”或“不变”)。
(4)实验结束时,乙同学发现收集到的氧气大于理论产量,针对这一现象,同学们进行了如下探究:
【提出猜想】
猜想I:反应生成的二氧化锰分解放出氧气;
猜想Ⅱ:反应生成的锰酸钾分解放出氧气。
【实验验证】同学们分为两组,分别进行以下实验:
①第一组同学取一定质量的二氧化锰装入试管,在250℃条件下加热一段时间,冷却后测得二氧化锰的质量不变.则猜想错误。
②第二组同学取锰酸钾装入试管,在250℃条件下加热,没有用测定质量的方法得出了猜想Ⅱ正确的结论.该组同学选择的实验方法是。