我们已经学过实验室制取气体的一般思路和方法,请利用下列装置回答相关问题.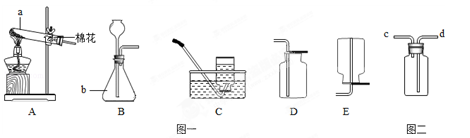
(1)写出图一中a和b的仪器名称:a b ;
(2)选择图一中的装置制取和收集二氧化碳气体,那么应选择的装置是 和 ;
在实验室中制取二氧化碳气体的常用药品:液体是 ,固体是 。
(3)若要用图二装置收集二氧化碳气体,则气体应从 (填c或d)端通.理由是 .
(4)用制取的二氧化碳进行如下有关性质实验:
①实验(II)中溶液变 色;
②实验(III)中加热之后,溶液又变为 色,解释出现此现象的原因 。
(5)实验室用高锰酸钾制取氧气的化学反应方程式(或化学式表达式) 若要用排水法收集一瓶较纯净的氧气,开始收集氧气的最佳时机是 。
(6)同学称取一定质量的KMnO4固体放入大试管中,将温度控制在250℃加热制取O2。实验结束时,乙同学发现用排水法收集到的O2大于理论产量。针对这一现象,同学们进行了如下探究:
[提出猜想]猜想I:反应生成的MnO2分解放出O2;
猜想II:反应生成的K2MnO4分解放出O2;
猜想III:反应生成的K2MnO4和MnO2分解都放出O2。
[实验验证]同学们分成两组,分别进行下列实验:
第一组同学取一定质量的MnO2,在250℃条件下加热一段时间,冷却后测得MnO2的质量不变,则猜想 错误;第二组同学取K2MnO4在250℃条件下加热,没有用测定质量的方法得出了猜想II正确的结论。该组同学选择的实验方法是 。
[拓展延伸]实验发现,KClO3固体加热制取O2的反应速率很慢,但如果将KMnO4固体与KClO3固体混合加热,则KClO3的分解速率大大加快。
请说明KMnO4在KClO3的分解反应中是否作催化剂,为什么? 。
类比法是化学研究物质的重要方法之一。草酸(C2H204)的化学性质与碳酸相似,草酸受热会分解得到三种氧化物,某兴趣小组对草酸的有关性质进行了探究,按要求回答相关的问题:
[提出猜想](1)草酸能够使紫色石蕊试液变为色。
(2)三种氧化物可能是,该猜想的依据是。
[查阅资料]
1.无水硫酸铜是一种白色粉末物质,遇水变成蓝色的硫酸铜晶体。
2.向氯化钯溶液中通入CO,产生黑色沉淀。
[实验探究]兴趣小组为验证猜想,将草酸受热后得到的气体,依次通过了装置A、B、C: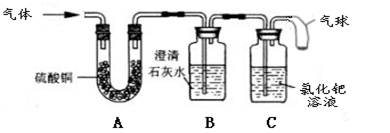
[实验结论](3)当装置A、B、C实验现象是,证明猜想是正确的。
[实验反思](4)①实验装置中气球所起的作用是。
②是否可以将装置A和B对调,其理由是。
如下图所示,将三支充满二氧化碳的试管分别倒立在盛有水、澄清石灰水、浓氢氧化钠溶液中进行实验,请按要求回答相关问题: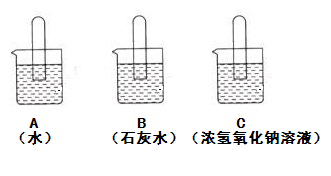
(提示:图示中呈现的是实验过程中的试管内液面的高度,不是最终的现象)
(1)B中的实验现象是,反应的化学方程式为。
(2)证明A中二氧化碳能与水反应的方法是。
(3)是否可以通过上述实验中的最终现象,证明二氧化碳能与氢氧化钠反应,其理由是。
(10分)某校研究性学习小组用右图装置进行镁条在空气中燃烧的实验:将镁条燃烧、冷却后打开止水夹。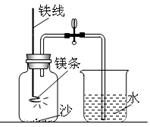
【发现问题】
进入集气瓶中水的体积约占集气瓶容积的30%。如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积应不超过其容积的%。可现进入集气瓶中水的体积约为其容积的30%,根据空气的组成,可推出减少的气体中一定有氮气,这种推测的理由是
。剩余约70%的气体主要成份是。
【提出假设】镁条能与空气中的氮气发生化学反应。
【探究实验】
接着上述实验,先拿开装置中集气瓶的胶塞,然后迅速把点燃的镁条伸进含有剩余气体的集气瓶中。发现镁条能在余下的气体中剧烈燃烧。
【实验结论】根据上述探究实验,你得的结论是。
【查阅资料】
①镁条在氮气中能燃烧并生成氮化镁(Mg3N2)固体。根据资料,氮化镁中氮元素的化合价,该反应的化学方程。
②镁条除了能与氮气反应,还可以在二氧化碳气体中燃烧生成碳和氧化镁。请你写出该反应的化学方程式。
【实验反思】通过以上探究,你对燃烧有了什么新的认识:
。(写出一点即可)。
(12分) 现有下列A、B、C、D、E五种实验装置,根据题意,将装置的序号填入下列空格中。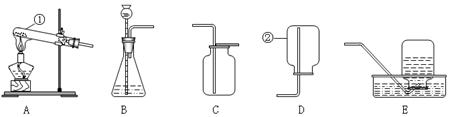
(1)写出指定仪器的名称:①;② 。
(2)用高锰酸钾制取氧气,气体发生装置选用(填序号);用高锰酸钾制取氧气的化学方程式为;
(3)用C装置收集CO2时,检验CO2是否收集满的方法是。
(4)用过氧化氢溶液制取氧气,气体发生装置选用(填序号);用过氧化氢溶液制取氧气的化学方程式为。
(5)氨气(NH3)无色、有刺激性气味,极易溶于水,密度比空气小;实验室常用加热固体硫酸铵和固体氢氧化钙的混合物来制取氨气(在制得氨气的同时还生成了硫酸钙和水)。则氨气的制取和收集的装置是(填序号); 请你写出该反应的化学方程式。
市售某品牌饮料的罐体是A1—Fe合金,为测定其中Al的质量分数,某学习小组精确称取0.050 g合金样品,设计了如下装置并进行实验: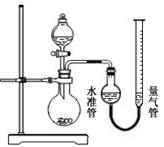
【查阅资料】:1、Al和NaOH溶液反应,放热并生成H2,反应中对应关系为2Al ~ 3H2,Fe和NaOH溶液不反应;2、实验条件下,H2的密度近似为0.090 g·L—1。
【实验步骤】:
①;②装入药品和水,连接装置;③记录量气管中水面读数为5 mL;④打开分液漏斗活塞,逐滴滴入NaOH溶液,至不再产生气泡为止,关闭活塞;⑤待温度降至室温时,记录量气管中水面读数为49 mL;⑥处理剩余药品,整理实验台。
【实验分析及数据处理】:
(1)完善实验步骤中的所缺部分;
(2)检查气密性的方法:打开分液漏斗活塞,向量气管中加入水,使水准管和量气管中水面相平,关闭活塞,降低量气管,若两侧水面高度差(填“改变”或“不变”),则气密性良好;
(3)实验结束后,读取量气管中水面刻度之前,需进行的操作是;
(4)计算此A1—Fe合金样品中Al的质量分数(3分,精确到小数点后3位);;
【实验反思】:
(5)造成实验结果偏大的原因可能是。
A.实验过程加入NaOH溶液的体积
B.没有冷却至室温就开始读数
C.装置漏气