(6分)关于氢气的性质有下面一段叙述:“在通常情况下,氢气是一种无色、无气味的气体,它难溶于水,它的密度约为空气密度的1/14。纯净的氢气能在空气中燃烧生成水,放出大量的热。将氢气通入盛有氧化铜的试管中,过一会加热试管,黑色的氧化铜变成光亮的铜”。根据上述内容,你可以知道:
(1)氢气具有的物理性质是: 。
(2)氢气具有的化学性质是: 。
(3)氢气可用于: 。
(1)用NaCl配制100mL 0.9%医用的生理盐水(密度约为1g/ cm3),需要NaCl的质量为g。
(2)由右图可知,t1℃时,硝酸钾溶解度氯化钠的溶解度(填“>”,“<”或“=”);从氯化钠和硝酸钾饱和溶液中提取硝酸钾,应采用下列方法中的(填写编号)。
a.冷却结晶 b.蒸发溶剂 c.过滤
食盐晶体是由下面三种粒子中的两种构成:
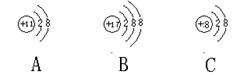 |
其中,B表示的粒子是; A与C形成化合物的化学式为。
下面是以井盐水为原料生产食盐及利用食盐生产某些化工产品的流程图示意图。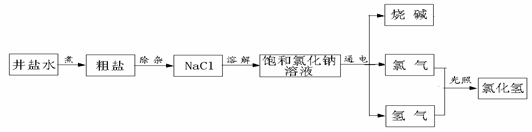
(1)写出上图中一种单质的化学式;
(2)产品氯化氢中氢元素的化合价为;
(3)从微观角度说明上面流程中“煮”的实质是。
如下图所示,回答下列问题: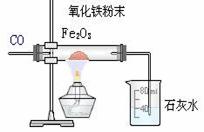
(1)实验开始后,大试管内有何变化?请写出此处发生反应的化学方程式?
(2)请指出这位同学所用实验装置的不足之处。
(3)实验结束后,请分析石灰水倒吸入试管中的原因是什么?
下图是硝酸钾溶解度曲线。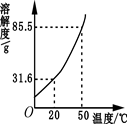
(1)硝酸钾溶液中的溶质是.
(2)从右图曲线可以得到的信息是(写一条即可)