已知某纯碱样品中含有NaCl杂质,为测定样品中纯碱的质量分数,甲同学用下图装置及试剂进行实验(夹持仪器略)。填写下列空白处。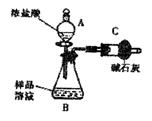
(1)仪器A、B的名称分别是  、 。
、 。
(2)甲同学按实验正常操作的主要步骤如下:
① ;
②将ag试样放入仪器B中,加适量蒸馏水溶解,得 到样品溶液;
到样品溶液;
③称量盛有碱石灰的干燥管的质量为bg;
④ 从仪器A中滴入浓盐酸,直到不再产生气体时为止;
从仪器A中滴入浓盐酸,直到不再产生气体时为止;
⑤再次称量盛有碱石灰的干燥管的质量为cg;
(3)甲同学根据以上实验求得的样品中Na2CO3的质量分数是 (用含a、b、c的式子表示)
(4)乙同学认为甲同学在实验装置设计和使用药品上都有缺陷,会导致测得的Na2CO3的质量分数偏高,而丙同学则认为甲同学的实验装置会使测得的结果偏低,丙同学认为结果偏低的原因可能是: 。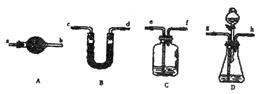
(5)若要解决乙、丙同学指出的甲同学实验中的问题,可对甲同学的实验装置和实验药品进行适当的改动,请按合理顺序选择仪器并完成下表:(用大写字母代表仪器,仪器可重复使用,夹持仪器略)
| 选用的仪器 |
|
|
|
|
|
| 添加的药品 及必要的操作 |
|
|
|
|
|
在一容积为3 L的密闭容器内加入0.3 mol的N2和0.9 mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)  2NH3 ΔH<0。反应中NH3的物质的量浓度的变化情况如图所示:
2NH3 ΔH<0。反应中NH3的物质的量浓度的变化情况如图所示:
(1)根据图示,计算从反应开始到平衡时,平均反应速率v(NH3)________。
(2)反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为()
a.0.20 mol/L b.0.12 mol/L c.0.10 mol/L d.0.08 mol/L
(3)反应达到平衡后,第5分钟末,保持其它条件不变,若只把容器的体积缩小一半,平衡移动(填“向逆反应方向”、“向正反应方向”或“不”),化学平衡常数_(填“增大”、“减小”或“不变”)
在一小烧杯里混合 10ml 0.01mol/L FeC13溶液和10ml
10ml 0.01mol/L FeC13溶液和10ml  0.01mol/L KSCN溶液,溶液立即变为红色。(1)再向溶液中滴入1mol/LFeC1
0.01mol/L KSCN溶液,溶液立即变为红色。(1)再向溶液中滴入1mol/LFeC1 3溶液,现象,平衡移动,KSCN浓度会。
3溶液,现象,平衡移动,KSCN浓度会。
(2)在烧杯中加入KC1固体,现象,平衡移动。(填“向逆反应方向”、“向正反应方向”或“不”)
下列方法中可以证明3H2+N2  2NH3已达平衡状态的是___ _____
2NH3已达平衡状态的是___ _____
①单位时间内生成n mol H2的同时生成n mol NH3
②一个H—H键断裂的同时有两个H—N键断裂
③百分组成N2%=NH3%④反应速率ν(H2)正=3ν(N2)逆时
⑤c(NH3) ∶ c(H2) ∶ c(N2)=2 ∶3∶ 1时
⑥温度和体积一定时,某一生成物浓度不再变化
⑦温度和体积 一定时容器内压强不再变化
一定时容器内压强不再变化
⑧条件一定,混合气体的平均相对分子质量不再变化
⑨条件一定,混合气体的总质量不再变化
有下列物质:①铜;②硫酸钡固体;③氢氧化钠固体;④氨水;⑤熔融硝酸钾;⑥乙醇;⑦液态HCl;⑧石墨;⑨二氧化硫;⑩冰醋酸; ⑾硫。
(1)其中能导 电的有________,其水溶液能导电的是________。
电的有________,其水溶液能导电的是________。
(2)属于非电解质的有________,属于强电解质的是________。
氢氧化铁胶体是中学中最重要的胶体,根据有关知识填空:
(1)实验室制备氢氧化铁胶体的方法是:取25mL蒸馏水,将其,向其中逐滴加入1~2mL,继续煮沸至,停止加热。
(2)将制备好的氢氧化铁胶体装入电泳装置,接通直流电,一段时间之后, ___极颜色加深。(填:“阴”或“阳”)
(3)向制备好的氢氧化铁胶体中逐滴加入硫酸能看到什么现象________(填序号)
A、生成大量沉淀 B、先沉淀再溶解 C、溶液澄清透明