I 铁及其化合物之间的相互转化可用下式表示:

回答下列有关问题:
(1)检验硫酸铁溶液中是否存在Fe2+的方法是___________________。
(2)干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2 = 2Na2FeO4+2Na2O+2Na2SO4+O2↑
该反应中的还原剂是___________,每生成l mol Na2FeO4转移____________mol电子。
(3)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:
Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①写出并配平湿法制高铁酸钾的离子反应方程式:_______________。
②若反应过程中转移了0.3 mol电子,则还原产物的物质的量为___________。
II某化学小组通过查阅资料,设计了如下图所示的方法以含镍废催化剂为原料来制备 。已知某化工厂的含镍废催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%)。
。已知某化工厂的含镍废催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%)。

部分阳离子以氢氧化物形式沉淀时的pH如下:

(1)“碱浸”过程中发生反应的离子方程式是
(2)“酸浸”时所加入的酸是 (填化学式)。
(3)加入H2O2时发生反应的离子方程式为
(4)操作b为调节溶液的pH,你认为pH的调控范围是
(5)NiS04·7Hz0可用于制备镍氢电池(NiMH),镍氢电池目前已经成为混合动力汽车的一种主要电池类型。NiMH中的M表示储氢金属或合金。该电池在充电过程中总反应的化学方程式是Ni(OH)2+M=NiOOH+MH,则NiMH电池放电过程中,正极的电极反应式为 。
(16分)乙酰水杨酸是一种使用广泛的解热镇痛剂。合成原理是:
(1)乙酰水杨酸的分子式为,1 mol乙酰水杨酸最多能与mol H2反应。
(2)上面反应的反应类型是。
(3)有关水杨酸的说法,不正确的是。
| A.能与溴水发生取代反应和加成反应 |
| B.可发生酯化反应和水解反应 |
| C.1 mol水杨酸最多能与2 mol NaOH反应 |
| D.遇FeCl3溶液显紫色 |
(4)乙酰水杨酸与足量KOH溶液反应的化学方程式为。
(5)乙酰氯(CH3COCl )也可以与水杨酸反应生成乙酰水杨酸,请写出化学反应方程式(不写条件)。
(6)写出一种符合下列条件的乙酰水杨酸的同分异构体的结构简式:。
Ⅰ.能遇FeCl3溶液显色
Ⅱ.苯环上只有2种一溴取代物
Ⅲ.1 mol该化合物能分别与含4 mol Br2的溴水或4 mol H2反应
〔化学—选修3:物质结构与性质〕(15分)已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于短周期。A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子最外层电子数是次外层电子数的3倍。E有“生物金属”之称,E4+和氩原子的核外电子排布相同。
请回答下列问题:
(1)B、C、D三种元素的电负性由小到大的顺序为,E的基态原子的电子排布式为。
(2)由B、D形成的BD32-离子中,其VSEPR模型名称是,离子的中心原子采用杂化。
(3)已知由A、C、D三种元素按照4:2:3的原子个数比可形成某离子化合物,常温下测得该离子化合物的水溶液pH=5,则该溶液中水电离出的氢离子浓度为。
(4)D、E和钡三种元素构成的某化合物的晶胞结构如图所示,该化合物的化学式为。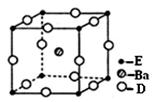
纳米级的EO2是一种广泛使用的催化剂,实验室往往通过ECl4在大量水中加热水解制得EO2·xH2O,该反应的化学方程式为。
〔化学—选修2:化学与技术〕(15分)Na2S2O3·5H2O可作为高效脱氯剂,工业上用硫铁矿(FeS2)为原料制备该物质的流程如下。
已知:I.气体A可以使品红溶液褪色,与硫化氢(H2S)混合能获得单质硫。
II.pH约为11的条件下,单质硫与亚硫酸盐可以共热生成硫代硫酸盐。
回答下列问题:
(1)沸腾炉中将粉碎的硫铁矿用空气吹动使之达到“沸腾”状态,其目的是。
(2)吸收塔中的原料B可以选用(填字母序号)。
A.NaCl溶液 B.Na2CO3溶液 C.Na2SO4溶液
(3)某小组同学用下图装置模拟制备Na2S2O3的过程(加热装置已略去)。
①A中使用70%的硫酸比用98%的浓硫酸反应速率快,其原因是。装置B的作用是。
②C中制备Na2S2O3发生的连续反应有:Na2S+H2O+SO2 = Na2SO3+H2S、和Na2SO3+S  Na2S2O3。
Na2S2O3。
(4)工程师设计了从硫铁矿获得单质硫的工艺,将粉碎的硫铁矿用过量的稀盐酸浸取,得到单质硫和硫化氢气体,该反应的化学方程式为。
乙二胺四乙酸可由乙二胺(H2NCH2CH2NH2)、氰化钠(NaCN)和甲醛水溶液作用制得,能和Fe3+形成稳定的水溶性配合物乙二胺四乙酸铁钠,原理如下:
(1)Fe3+基态核外电子排布式为。
(2)与CN-互为等电子体的一种非极性分子为(填化学式)。
(3)乙二胺四乙酸中C原子的轨道杂化类型是;C、N、O三种元素的第一电离能由大到小的顺序是。
(4)乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高得多,原因是。
(5)请在乙二胺四乙酸铁钠结构图中用“箭头”表示出配位键。
镁铝碱式碳酸盐[MgaAlb(OH)c(CO3)d·xH2O]阻燃剂具有阻燃、消烟、填充等功能,是一种不溶于水的新型无机阻燃剂。
(1)将MgaAlb(OH)c(CO3)d·xH2O表示成氧化物形式。
(2)为确定镁铝碱式碳酸盐的组成,进行如下实验:
准确称取15.050 g样品进行灼烧至恒重,生成CO2 0.560 L(已换算成标准状况下)。分析测得残留物中MgO为6.000 g,Al2O3为2.550 g,通过计算确定该镁铝碱式碳酸盐的化学式。(写出计算过程)
(3)该镁铝碱式碳酸盐可以由MgCl2、NaAlO2、NaOH和Na2CO3反应制备,制备的化学方程式为。